题目内容
海水中有非常丰富的化学资源,从海水中可提取多种化工原料.如图是某工厂对海水资源综合利用的示意图.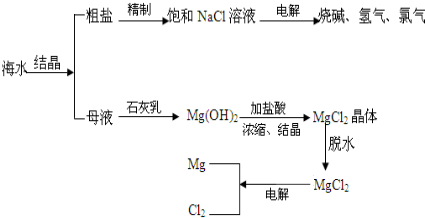
(1)粗盐中含有泥砂、CaCl2、MgCl2等杂质.实验室用粗盐配制不含杂质的饱和NaCl溶液,做了以下实验:
步骤一:除去泥砂.应进行的操作是:溶解、
步骤二:除去CaCl2和MgCl2.加入NaOH溶液,使MgCl2转化为Mg(OH)2,加入Na2CO3溶液,使CaCl2转化为CaCO3,为了除尽杂质,所加的NaOH和Na2CO3都需过量,在过滤除去Mg(OH)2和CaCO3沉淀后,应再加入适量的
(2)电解饱和食盐水后得到的溶液中含有NaOH和NaCl两种溶质,为了得到NaOH溶液,可用蒸发结晶的办法除去NaCl,这是因为
(3)海水提取粗盐后的母液中含KCl、MgCl2、NaCl等溶质,加入石灰乳后可得Mg(OH)2,而制石灰乳的原料可利用海滩上的贝壳(主要成分是CaCO3),写出由贝壳制取石灰乳有关反应的化学方程式:
①
(4)在两条生产流程中,在电解前对粗盐和母液进行处理的目的是一致的,都是
分析:(1)根据泥沙不溶于水而其他盐均溶于水得出结论;所加过量的NaOH和Na2CO3用盐酸除去,既不引入杂质离子,又达到除杂的效果;
(2)根据氯化钠的溶解度随温度变化不大的特征进行分析;
(3)碳酸钙在高温的条件下生成氧化钙和二氧化碳,氧化钙和水生成氢氧化钙;
(4)在两条生产流程中,粗盐和母液中有大量的杂质存在,所以必须进行除杂处理,然后电解得到相应的产物.
(2)根据氯化钠的溶解度随温度变化不大的特征进行分析;
(3)碳酸钙在高温的条件下生成氧化钙和二氧化碳,氧化钙和水生成氢氧化钙;
(4)在两条生产流程中,粗盐和母液中有大量的杂质存在,所以必须进行除杂处理,然后电解得到相应的产物.
解答:解:(1)根据泥沙不溶于水而其他盐均溶于水,故采用先溶解后过滤的方法;用盐酸除去过量的NaOH和Na2CO3,既不引入杂质离子,又达到除杂的效果;
(2)因为氯化钠的溶解度随温度变化不大,,所以可以采用蒸发溶剂法结晶,除去氢氧化钠中的氯化钠;
(3)CaCO3
CaO+CO2↑,CaO+H2O=Ca(OH)2;
(4)粗盐和母液中有大量的杂质存在,所以必须进行除杂处理.
故答案为:(1)过滤、盐酸
(2)氯化钠的溶解度随温度变化不大
(3)CaCO3
CaO+CO2↑;CaO+H2O=Ca(OH)2
(4)除杂.
(2)因为氯化钠的溶解度随温度变化不大,,所以可以采用蒸发溶剂法结晶,除去氢氧化钠中的氯化钠;
(3)CaCO3
| ||
(4)粗盐和母液中有大量的杂质存在,所以必须进行除杂处理.
故答案为:(1)过滤、盐酸
(2)氯化钠的溶解度随温度变化不大
(3)CaCO3
| ||
(4)除杂.
点评:本题是一道综合性试题,涉及知识点比较多,要求学生有完整的知识结构和分析问题的能力并对课本知识能够牢固的掌握.

练习册系列答案
 学而优暑期衔接南京大学出版社系列答案
学而优暑期衔接南京大学出版社系列答案 Happy holiday欢乐假期暑假作业广东人民出版社系列答案
Happy holiday欢乐假期暑假作业广东人民出版社系列答案
相关题目
 镁将成为21世纪重要的轻型环保材料,我国含有非常丰富的镁资源.
镁将成为21世纪重要的轻型环保材料,我国含有非常丰富的镁资源.(1)占地球表面积70%的海洋是天然的镁元素宝库,从海水中提取镁的流程如下:
海水中的MgCl2
| 熟石灰 |
| 过滤 |
| 盐酸 |
| 蒸发、浓缩、结晶 |
| 脱水 |
| 通电 |
①在实验室进行过滤操作时需要用到玻璃棒,其作用是
②电解熔融氯化镁的过程中,
(2)①金属镁是一种较活泼金属,在二氧化碳气体中也能燃烧.燃烧的化学方程式为2Mg+C02═C+2MgO,此反应类型属于
A.分解反应 B.化合反应 C.置换反应 D.复分解反应
②金属镁在高温下与氮气反应生成氮化镁,在氮化镁中氮元素的化合价为一3.据此写出氮化镁的化学式
(3)镁铝合金广泛用于火箭、导弹和飞机制造业等.某兴趣小组为探究镁铝合金的组成,取16g镁铝合金样品,把60g氢氧化钠溶液平均分成三份依次加入样品中(铝与氢氧化钠溶液反应的化学方程式为2Al+2NaOH+2H2O═2NaAl02+3H2↑,镁与氢氧化钠溶液不反应),充分反应后,过滤出固体,将其洗涤、干燥、称量,得实验数据如下:
| 所加氢氧化钠溶液的次数 | 第一次 | 第二次 | 第三次 |
| 剩余固体的质量/g | 10.6 | 5.2 | 4.O |
(4)老师每次做有关镁的实验时都会强调:镁是一种银白色有金属光泽的金属.但拿出的镁条总是有一层灰黑色的“外衣“,这层灰黑色的外衣是什么物质呢?
猜想:小明认为可能是MgO;小赵认为可能是Mg2(OH)2C03;小花认为可能是Mg(OH)2.
小赵认为小明的猜想是错误的,其理由是
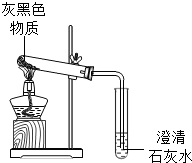
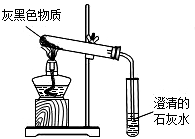
实验探究:小赵按如图所示装置进行实验,发现试管口有液滴出现,澄清石灰水变浑浊,同时试管内生成白色固体.
实验分析:实验后,小赵认为小花的猜测也是错误的,
其理由是
查阅资料得出结论:Mg(OH)2和Mg2(OH)2C03都可以加热分解,产物均为氧化物,据此请你写出Mg2(OH)2C03
加热分解的化学方程式

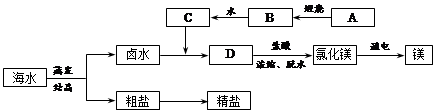


 C+2MgO ,此反应类型属于_____
C+2MgO ,此反应类型属于_____