题目内容
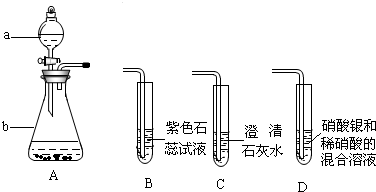
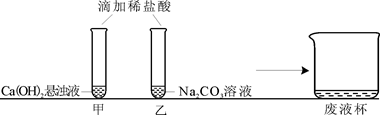
实验室用如图装置制取干燥纯净的CO2气体,并验证CO2中混有HCl气体(假设每步反应均完全反应).
(1)写出实验室制取二氧化碳的化学方程式______;
(2)D装置的作用是______,D装置中的现象是______.
(3)将上图装置按题目要求连接起来,正确顺序是:______(填连接字母序号).

(1)写出实验室制取二氧化碳的化学方程式______;
(2)D装置的作用是______,D装置中的现象是______.
(3)将上图装置按题目要求连接起来,正确顺序是:______(填连接字母序号).
(1)实验室通常用稀盐酸与大理石(或石灰石)反应制取二氧化碳,碳酸钙与盐酸反应生成氯化钙、水和二氧化碳,反应的方程式:CaCO3+2HCl=CaCl2+H2O+CO2↑;
(2)由于氯化氢气体溶于水得到盐酸,通过硝酸银溶液来检验氯离子,来验证并验证CO2中混有HCl气体,所以,D装置的作用是验证CO2中混有HCl气体,D装置中发生的化学反应方程式是 HCl+AgNO3=HNO3+AgCl↓;故D装置中的现象是产生白色沉淀;
(3)由于实验室要制取干燥纯净的CO2气体,应先除去混有HCl气体,再干燥,最后收集.所以,将上图装置按题目要求连接起来,正确顺序是:aefbcd.
故答为:(1)CaCO3+2HCl=CaCl2+H2O+CO2↑;(2)验证CO2中混有HCl气体;产生白色沉淀;(3)aefbcd.
(2)由于氯化氢气体溶于水得到盐酸,通过硝酸银溶液来检验氯离子,来验证并验证CO2中混有HCl气体,所以,D装置的作用是验证CO2中混有HCl气体,D装置中发生的化学反应方程式是 HCl+AgNO3=HNO3+AgCl↓;故D装置中的现象是产生白色沉淀;
(3)由于实验室要制取干燥纯净的CO2气体,应先除去混有HCl气体,再干燥,最后收集.所以,将上图装置按题目要求连接起来,正确顺序是:aefbcd.
故答为:(1)CaCO3+2HCl=CaCl2+H2O+CO2↑;(2)验证CO2中混有HCl气体;产生白色沉淀;(3)aefbcd.

练习册系列答案
相关题目