题目内容
【题目】实验小组研究盐酸、氢氧化钙两种物质的化学性质,做了如下图所示实验。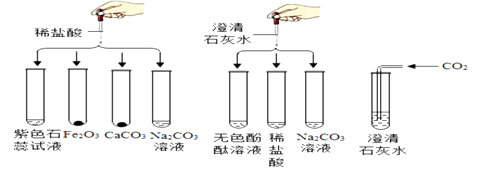
(1)实验后某试管中为红色溶液,向其中加入足量的 , 溶液变为无色。由此推断,该试管中最初盛有的物质是。
(2)实验后某试管的底部有白色固体,过滤后向滤液中滴加稀盐酸,一段时间后有气泡出现。由此推断,该试管中最初发生反应的化学方程为。
(3)实验后某试管中只得到无色溶液,向其中加入足量的Na2CO3溶液,无明显现象。由此推断,原试管所得无色溶液中的溶质一定有。
【答案】
(1)稀盐酸,无色酚酞溶液
(2)Na2CO3+Ca(OH)2=CaCO3↓+2NaOH
(3)NaCl
【解析】(1)实验后某试管中为红色溶液,向其中加入足量的稀盐酸,溶液变为无色。由此推断,该试管中最初盛有的物质是无色酚酞溶液;
(2)实验后某试管的底部有白色固体,过滤后向滤液中滴加稀盐酸,一段时间后有气泡出现。由此推断,该试管中最初发生反应的化学方程为Na2CO3+Ca(OH)2=CaCO3↓+2NaOH;
(3)实验后某试管中只得到无色溶液,向其中加入足量的Na2CO3溶液,无明显现象。由此推断,原试管所得无色溶液中的溶质一定有NaCl,氢氧化钠和盐酸反应生成氯化钠.
所以答案是:(1)稀盐酸;无色酚酞溶液;(2)Na2CO3+Ca(OH)2=CaCO3↓+2NaOH;(3)NaCl.
【考点精析】本题主要考查了书写化学方程式、文字表达式、电离方程式的相关知识点,需要掌握注意:a、配平 b、条件 c、箭号才能正确解答此题.

练习册系列答案
 高中必刷题系列答案
高中必刷题系列答案
相关题目