题目内容
在一定条件下,在一个密闭容器内发生某个反应,测得反应过程中各物质的质量如下表所示,则B与C的变化质量比为 ;该反应的基本类型为 .
| 物质 | A | B | C | D |
| 反应前质量/g | 10 | 10 | 10 | 2 |
| 反应后质量/g | 待测 | 2 | 21 | 2 |
考点:质量守恒定律及其应用,反应类型的判定
专题:化学用语和质量守恒定律
分析:根据表中的数据和质量守恒定律进行分析.反应中,反应物质量会减少,生成物质量会增加,从而判断生成物与反应物,再利用质量关系进行求解.
解答:解:由表中的数据可知:根据质量守恒定律,10g+10g+10g+2g=待测+2g+21g+2g,因此反应后A的质量为7g;则C的质量增加,是生成物;A、B的质量减少,是反应物;D的质量不变;B和C两种物质变化的质量比为:(10g-2g):(21g-10g)=8:11;
该反应中C是生成物;A、B是反应物,该反应符合“多变一”,所属的基本反应类型是化合反应.
故答案为:
8:11;化合反应
该反应中C是生成物;A、B是反应物,该反应符合“多变一”,所属的基本反应类型是化合反应.
故答案为:
8:11;化合反应
点评:此题是有关质量守恒定律的考查题,解题的关键是利用质量守恒定律对相关量的分析与判断,并进而对反应的类型及质量关系进行探讨.

练习册系列答案
 名师点拨卷系列答案
名师点拨卷系列答案
相关题目
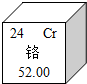 2012年4月16日新华社电,由于涉嫌铬超标,国家食品药品监督管理局发出紧急通知,要求对13个药用空心胶囊产品暂停销售和使用.铬,是一种毒性很大的重金属,在人体内蓄积具有致癌性并可能诱发基因突变.铬为不活泼性金属,在常温下对氧和湿气都是稳定的,铬很容易和稀盐酸或稀硫酸反应,生成氯化物或硫酸盐,同时放出氢气.铬元素相关信息如图所示.下列说法中,不正确的是( )
2012年4月16日新华社电,由于涉嫌铬超标,国家食品药品监督管理局发出紧急通知,要求对13个药用空心胶囊产品暂停销售和使用.铬,是一种毒性很大的重金属,在人体内蓄积具有致癌性并可能诱发基因突变.铬为不活泼性金属,在常温下对氧和湿气都是稳定的,铬很容易和稀盐酸或稀硫酸反应,生成氯化物或硫酸盐,同时放出氢气.铬元素相关信息如图所示.下列说法中,不正确的是( )| A、铬原子核内有24个质子 |
| B、铬的相对原子质量为52.00 |
| C、铬性质不活泼,因此食品中铬超标,不影响健康 |
| D、若把铬放入金属活动性表中,它必排在H的前面 |
下列物质间的转化,不能通过一步反应实现的是( )
| A、CO2→CaCO3 |
| B、CO→CO2 |
| C、H2O2→O2 |
| D、Cu→Cu(OH)2 |
下列变化中,属于物理变化的是( )
| A、食物腐败 | B、纸张燃烧 |
| C、石蜡熔化 | D、钢铁生锈 |
下列方法不能达到目的是( )
| A、用加热的方法除掉Na2CO3中混入的NaOH |
| B、加入适量盐酸可以除掉氯化钠溶液中混入的氢氧化钠 |
| C、将一氧化碳、二氧化碳的混合气体通入灼热的氧化铜可除掉一氧化碳 |
| D、加入足量的铁粉可除去硫酸亚铁溶液中混入的少量硫酸 |
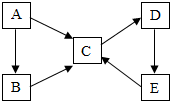 A、B、C、D、E均为初中化学常见的物质,它们之间的转化关系如图所示(其中“→”表示某一种物质经一步反应可转化为另一种物质,部分反应物、生成物和反应条件已略去).
A、B、C、D、E均为初中化学常见的物质,它们之间的转化关系如图所示(其中“→”表示某一种物质经一步反应可转化为另一种物质,部分反应物、生成物和反应条件已略去).