题目内容
【题目】下图烧杯中装有100g稀盐酸和氯化镁的混合溶液,向该溶液中加入10%的氢氧化钠溶液至恰好完全反应时,生成沉淀2.9g。请回答:
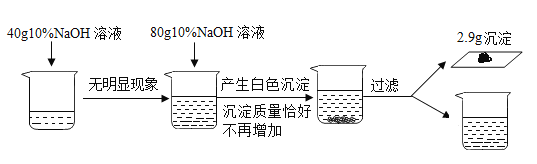
(1)写出实验中产生沉淀的化学方程式_______________。
(2)列出求解原混合溶液中含有氯化镁质量(x)的比例式_______________。
(3)第一次实验后所得溶液中溶质的化学式为_______________。
(4)该混合溶液中氯化氢和氯化镁的质量比为_______________。
(5)向过滤后所得溶液中加入82. 9g水后,所得溶液中溶质质量分数为_______________。
【答案】(1)![]() (2)
(2)![]() (3)HCl、NaCl、MgCl2(4)146:95(5)5. 85%
(3)HCl、NaCl、MgCl2(4)146:95(5)5. 85%
【解析】
(1)实验中产生沉淀的化学反应是氢氧化钠和氯化镁反应生成氢氧化镁沉淀和氯化钠,其化学方程式为:![]() 。
。
(2)已知沉淀量为2.9g,设氯化镁的质量的为x,和氯化镁反应的氢氧化钠的质量为a,
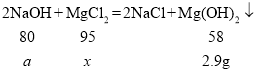
则比例式为![]() ,解得x=4.75g,
,解得x=4.75g,
![]() ,解得a=4g。
,解得a=4g。
(3)第一次实验后无明显现象,说明氯化镁未参加反应,而是氢氧化钠和稀盐酸反应生成了氯化钠和水,由上分析可知,与氯化镁反应生成沉淀的氢氧化钠消耗为4g,而第二次加入了80g10%的氢氧化钠溶液(含有氢氧化钠80g×10%=8g)恰好完全反应,说明第二次加入的氢氧化钠溶液中还有4g氢氧化钠和稀盐酸反应,所得溶液中含有稀盐酸,则溶质的化学式为HCl、NaCl、MgCl2。
(4)根据第二问可知,氯化镁的质量为4.75g,两次和稀盐酸反应共消耗80g×10%=8g(第一次4g和第二次的4g)的氢氧化钠,设稀盐酸的质量为y
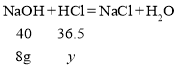
![]()
y=7.3g
该混合溶液中氯化氢和氯化镁的质量比为![]() 146:95。
146:95。
(5)过滤后的溶液为氯化钠溶液,根据钠元素守恒,所有的氢氧化钠(40×10%+80×10%=12g)全部转化为氯化钠,设生成氯化钠的质量为z,根据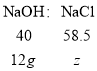 ,则
,则![]() ,z=17.55g,向过滤后所得溶液中加入82. 9g水后,所得溶液中溶质质量分数为
,z=17.55g,向过滤后所得溶液中加入82. 9g水后,所得溶液中溶质质量分数为![]() =5. 85%。
=5. 85%。

 七彩题卡口算应用一点通系列答案
七彩题卡口算应用一点通系列答案【题目】阅读下面科普短文
碳元素是最早被人类认识和利用的元素。碳元素在地球上虽然广泛分布,但其含量不足 0.03%。
碳元素是一切有机体骨架的组成元素,在人体中的含量约占 18%。主要以有机含碳化合物形式存在,如糖类、蛋白质等。人体中的无机含碳化合物种类较少,在血浆中主要以碳酸氢盐缓冲系统(H2CO3/HCO3-)的形式存在,人体细胞通过有氧氧化和无氧酵解产生的二氧化碳,是碳元素在人体内的另一种无机形式。
迄今为止,发现了 15 种碳原子,它们在元素周期表中占据如图 1 所示的同一个“格”,其中 C-12 和 C-13 属于稳定型,考古研究中,通过测定 C-14 含量估算古物的年代。
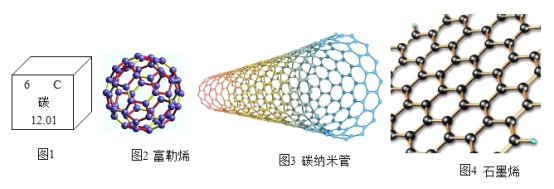
20世纪起,人类对碳元素的认识突飞猛进。下表列出了与之相关的主要事件。碳的这些新型结构的发现和性能研究的发展,使其广泛应用于工业、材料、生物医学等领域。依据文章内容回答下列问题:
时间 | 40 年代 | 1967 年 | 1969 年 | 1985 年 | 1991 年 | 21 世纪 |
事件 | 发现C-14 | 发现六角金刚石和单斜超硬碳 | 发现银白色的白炭 | 发现富勒烯的第一个成员C60(图 2) | 发现碳纳米管(图 3) | 从石墨中剥离出仅由一层碳原子构成的薄片-石墨烯(图 4) |
(1)碳在人体中的存在形式有______________________种。
(2)结合你所学的知识,你认为 C-12 和 C-13 的不同点是______________________。
A 质子数不同 B 电子数不同 C 中子数不同
(3)C60 的含义是______________________。