题目内容
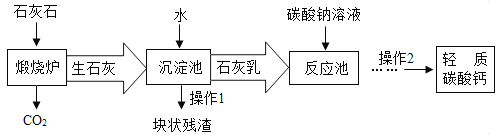
【题目】勇往直前学习小组的同学们在实验室中模拟我国古代劳动人民湿法冶金实验,过程如图所示,已知铁粉中杂质不溶于水,也不与其他物质反应,请回答:
(1)写出铁与硫酸铜溶液反应的化学方程式;
(2)根据硫酸铜质量列出求解样品中铁的质量(x)的比例式;
(3)如果用25%的硫酸铜溶液加水稀释来配制实验中需要的160g10%的硫酸铜溶液,需要用25%的硫酸铜溶液的质量是;
(4)图中a的数值为;
(5)最后得到的不饱和溶液M中溶质的质量分数为。
【答案】
(1)Fe+CuSO4=Cu+FeSO4
(2)56:X=160:(160克×10%)
(3)64g
(4)6.8
(5)7.6%
【解析】铁与硫酸铜溶液反应的化学方程式Fe+CuSO4=Cu+FeSO4 , 设样品中铁的质量为x,生成的铜和硫酸亚铁的质量分别z和c,
Fe + | CuSO4 = | Cu + | FeSO4 |
56 | 160 | 64 | 152 |
x | 160g×10% | z | c |
列比例式得56:x=160:(160克×10%)=64:z=152:c,
求得z=6.4g,x=5.6g c=15.2g
设需要用25%的硫酸铜溶液的质量是Y,则25%Y=160克×10% 解得Y=64克,a的质量=6.4克+(6克-5.6克)=6.8克,最后得到的不饱和溶液M中溶质的质量分数为=15.2克/(160克+5.6克+40.8克-6.4克)×100%=7.6%。
所以答案是:(1)Fe+CuSO4=Cu+FeSO4;(2)56:X=160:(160克×10%)(3)64g(4)6.8(5)7.6%
【考点精析】关于本题考查的书写化学方程式、文字表达式、电离方程式,需要了解注意:a、配平 b、条件 c、箭号才能得出正确答案.

练习册系列答案
 智慧课堂密卷100分单元过关检测系列答案
智慧课堂密卷100分单元过关检测系列答案
相关题目