题目内容
有一瓶固体氯化钾,其中含有少量氯化钡.某同学取出一部分,将它溶于水溶液,并分装在甲、乙两支试管中,进行以下实验:实验一:在甲试管中逐滴加入稀硫酸,至不再产生沉淀,过滤,在滤液中加入氢氧化钾溶液至中性,加热浓缩,冷却得到固体A.实验二:在乙试管中逐滴加入碳酸钾溶液,至不再生成沉淀,过滤,在滤液中加入盐酸至酸性,加热浓缩,冷却得到固体B.请回答哪一实验方法制得的氯化钾纯一些?为什么?
【答案】分析:可以根据物质的性质方面进行分析、判断,从而得出正确的结论.如第一种方法,加入稀硫酸后发生的反应包括:氯化钡和稀硫酸生成硫酸钡沉淀和氯化氢,再加氢氧化钾和氯化氢反应生成氯化钾和水,但若稀硫酸加的多还会与氢氧化钾反应得到硫酸钾和水,故最终得到固体中含有氯化钾和少量的硫酸钾.
解答:解:第一种方法,加入稀硫酸后发生的反应包括:氯化钡和稀硫酸生成硫酸钡沉淀和氯化氢,再加氢氧化钾和氯化氢反应生成氯化钾和水,但若稀硫酸加的多还会与氢氧化钾反应得到硫酸钾和水,故最终得到固体中含有氯化钾和少量的硫酸钾.
第二种方法,加入碳酸钾氯化钡和它反应但氯化钾不反应,氯化钡和碳酸钾反应生成碳酸钡沉淀和氯化钾,故过滤后溶液中溶质含有氯化钾不含氯化钡,含有多余的碳酸钾,加入盐酸至酸性,碳酸钾和盐酸反应生成氯化钾和水还有二氧化碳气体,加热浓缩氯化氢会蒸发,冷却得到纯净的固体氯化钾.因为第一种方法中加入硫酸只有略过量才不再产生沉淀,使最终所得固体A中含有K2SO4;第二种方法中过量的碳酸钾被盐酸除掉而转化成KCl,多余的盐酸在蒸发过程中以HCl气体挥发掉.
故答案:第二种方法纯些.
点评:解答本题的关键是要充分理解各种物质的性质,只有这样才能对问题做出正确的判断.
解答:解:第一种方法,加入稀硫酸后发生的反应包括:氯化钡和稀硫酸生成硫酸钡沉淀和氯化氢,再加氢氧化钾和氯化氢反应生成氯化钾和水,但若稀硫酸加的多还会与氢氧化钾反应得到硫酸钾和水,故最终得到固体中含有氯化钾和少量的硫酸钾.
第二种方法,加入碳酸钾氯化钡和它反应但氯化钾不反应,氯化钡和碳酸钾反应生成碳酸钡沉淀和氯化钾,故过滤后溶液中溶质含有氯化钾不含氯化钡,含有多余的碳酸钾,加入盐酸至酸性,碳酸钾和盐酸反应生成氯化钾和水还有二氧化碳气体,加热浓缩氯化氢会蒸发,冷却得到纯净的固体氯化钾.因为第一种方法中加入硫酸只有略过量才不再产生沉淀,使最终所得固体A中含有K2SO4;第二种方法中过量的碳酸钾被盐酸除掉而转化成KCl,多余的盐酸在蒸发过程中以HCl气体挥发掉.
故答案:第二种方法纯些.
点评:解答本题的关键是要充分理解各种物质的性质,只有这样才能对问题做出正确的判断.

练习册系列答案
相关题目
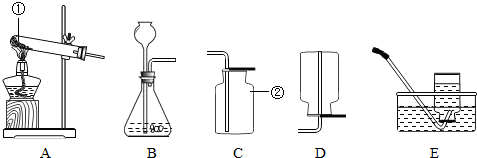
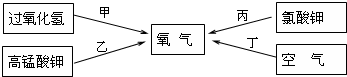
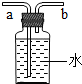

 实验室常用于制取氧气的方法有:a、加热氯酸钾晶体和二氧化锰粉末;b、加热高锰酸钾固体;c、用二氧化锰粉末作催化剂使过氧化氢(H2O2)溶液分解产生水和氧气.
实验室常用于制取氧气的方法有:a、加热氯酸钾晶体和二氧化锰粉末;b、加热高锰酸钾固体;c、用二氧化锰粉末作催化剂使过氧化氢(H2O2)溶液分解产生水和氧气.