题目内容
化学无处不在,与人类的生产、生活密切联系,人类社会离不开化学.请你利用下列物质:①二氧化硅 ②Fe2O3③MgCl2④氨气 ⑤盐酸 ⑥氢气 ⑦食盐水 ⑧纯碱 ⑨二氧化碳 ⑩Ca(OH)2,结合所学知识,回答下列问题:(1)大多数的植物适宜在接近中性的土壤中生长.正确测得某地土壤的浸出液的pH<4,作物不能正常生长,我们可以向土壤中加入(填序号) 改良.
(2)做面条时,面团因较长时间储存而有酸味,常加入适量的(填序号) 中和.
(3)海洋是人类宝贵资源,人类可以提取海水的各种元素,来大量制备对我们有用的物质,写出从海水提取镁过程中涉及到的方程式: ;氨碱法制纯碱过程中涉及到的方程式: .
(4)玻璃是我们日常生活中常用的物质.写出制造玻璃过程中涉及到的方程式:
.
(5)工人师傅在焊接金属时,常常先除去表面的铁锈,写出除去铁锈的方程式:
.
(6)氢气是未来最理想的能源,具有广阔的开发前景,目前只在火箭发射等少数情况下使用,不能广泛使用,主要原因是 (答出一条即可).
(7)铵态氮肥不能和Ca(OH)2混合施用的原因是 .
【答案】分析:(1)根据氢氧化钙显碱性,可用于改良酸性土壤进行解答;
(2)根据碳酸钠溶于水显碱性,可以与发酵酸反应生成二氧化碳进行解答;
(3)根据海水提取镁的原理以及氨碱法制纯碱的方法进行解答;
(4)根据碳酸钠、碳酸钙和二氧化硅反应进行解答;
(5)根据盐酸和氧化铁反应生成氯化铁和水进行解答;
(6)根据氢气不能广泛使用的原因进行解答;
(7)根据铵态氮肥与碱发生反应放出氨气进行解答.
解答:解:(1)氢氧化钙显碱性,可用于改良酸性土壤;
(2)碳酸钠溶于水显碱性,可以与发酵酸反应生成二氧化碳;
(3)海水提取镁过程:氢氧化钙和氯化镁反应生成氢氧化镁沉淀和氯化钙,然后过滤后盐酸和氢氧化镁反应生成氯化镁和水,再通电分解氯化镁得到金属镁和氯气.其中涉及到的方程式:MgCl2+Ca(OH)2=Mg(OH)2↓+CaCl2;Mg(OH)2+2HCl=MgCl2+2H2O;MgCl2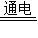 Mg+Cl2↑;氨碱法制纯碱过程是在氨盐水中通入二氧化碳生成氯化铵和碳酸氢钠,其中涉及到的方程式:NaCl+NH3+CO2+H2O=NaHCO3+NH4Cl;
Mg+Cl2↑;氨碱法制纯碱过程是在氨盐水中通入二氧化碳生成氯化铵和碳酸氢钠,其中涉及到的方程式:NaCl+NH3+CO2+H2O=NaHCO3+NH4Cl;
(4)制造玻璃过程中是碳酸钠、碳酸钙和二氧化硅反应生成硅酸钠和硅酸钙以及二氧化碳,涉及到的方程式:Na2CO3+SiO2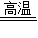 Na2SiO3+CO2↑;CaCO3+SiO2
Na2SiO3+CO2↑;CaCO3+SiO2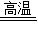 CaSiO3+CO2↑;
CaSiO3+CO2↑;
(5)盐酸和氧化铁反应生成氯化铁和水,化学方程式:Fe2O3+6HCl=2FeCl3+3H2O;
(6)氢气是未来最理想的能源,具有广阔的开发前景,目前只在火箭发射等少数情况下使用,不能广泛使用,主要原因是:制备氢气消耗电能大,成本高(或没有寻找到合适的光分解催化剂,使水分解或没有发现安全贮存氢气的方法等);
(7)铵态氮肥不能和Ca(OH)2混合施用的原因是:铵态氮肥与碱发生反应放出氨气,肥效降低.
故答案为:(1)⑩;(2)⑧;(3)MgCl2+Ca(OH)2=Mg(OH)2↓+CaCl2;Mg(OH)2+2HCl=MgCl2+2H2O;MgCl2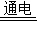 Mg+Cl2↑;NaCl+NH3+CO2+H2O=NaHCO3+NH4Cl;(4)Na2CO3+SiO2
Mg+Cl2↑;NaCl+NH3+CO2+H2O=NaHCO3+NH4Cl;(4)Na2CO3+SiO2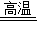 Na2SiO3+CO2↑;CaCO3+SiO2
Na2SiO3+CO2↑;CaCO3+SiO2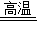 CaSiO3+CO2↑;(5)Fe2O3+6HCl=2FeCl3+3H2O;(6)制备氢气消耗电能大,成本高;(7)铵态氮肥与碱发生反应放出氨气,肥效降低.
CaSiO3+CO2↑;(5)Fe2O3+6HCl=2FeCl3+3H2O;(6)制备氢气消耗电能大,成本高;(7)铵态氮肥与碱发生反应放出氨气,肥效降低.
点评:本题考查利用课本知识解决新问题能力,能加深学生对课本知识的理解,训练学生的思维能力.
(2)根据碳酸钠溶于水显碱性,可以与发酵酸反应生成二氧化碳进行解答;
(3)根据海水提取镁的原理以及氨碱法制纯碱的方法进行解答;
(4)根据碳酸钠、碳酸钙和二氧化硅反应进行解答;
(5)根据盐酸和氧化铁反应生成氯化铁和水进行解答;
(6)根据氢气不能广泛使用的原因进行解答;
(7)根据铵态氮肥与碱发生反应放出氨气进行解答.
解答:解:(1)氢氧化钙显碱性,可用于改良酸性土壤;
(2)碳酸钠溶于水显碱性,可以与发酵酸反应生成二氧化碳;
(3)海水提取镁过程:氢氧化钙和氯化镁反应生成氢氧化镁沉淀和氯化钙,然后过滤后盐酸和氢氧化镁反应生成氯化镁和水,再通电分解氯化镁得到金属镁和氯气.其中涉及到的方程式:MgCl2+Ca(OH)2=Mg(OH)2↓+CaCl2;Mg(OH)2+2HCl=MgCl2+2H2O;MgCl2
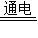 Mg+Cl2↑;氨碱法制纯碱过程是在氨盐水中通入二氧化碳生成氯化铵和碳酸氢钠,其中涉及到的方程式:NaCl+NH3+CO2+H2O=NaHCO3+NH4Cl;
Mg+Cl2↑;氨碱法制纯碱过程是在氨盐水中通入二氧化碳生成氯化铵和碳酸氢钠,其中涉及到的方程式:NaCl+NH3+CO2+H2O=NaHCO3+NH4Cl;(4)制造玻璃过程中是碳酸钠、碳酸钙和二氧化硅反应生成硅酸钠和硅酸钙以及二氧化碳,涉及到的方程式:Na2CO3+SiO2
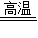 Na2SiO3+CO2↑;CaCO3+SiO2
Na2SiO3+CO2↑;CaCO3+SiO2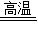 CaSiO3+CO2↑;
CaSiO3+CO2↑;(5)盐酸和氧化铁反应生成氯化铁和水,化学方程式:Fe2O3+6HCl=2FeCl3+3H2O;
(6)氢气是未来最理想的能源,具有广阔的开发前景,目前只在火箭发射等少数情况下使用,不能广泛使用,主要原因是:制备氢气消耗电能大,成本高(或没有寻找到合适的光分解催化剂,使水分解或没有发现安全贮存氢气的方法等);
(7)铵态氮肥不能和Ca(OH)2混合施用的原因是:铵态氮肥与碱发生反应放出氨气,肥效降低.
故答案为:(1)⑩;(2)⑧;(3)MgCl2+Ca(OH)2=Mg(OH)2↓+CaCl2;Mg(OH)2+2HCl=MgCl2+2H2O;MgCl2
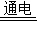 Mg+Cl2↑;NaCl+NH3+CO2+H2O=NaHCO3+NH4Cl;(4)Na2CO3+SiO2
Mg+Cl2↑;NaCl+NH3+CO2+H2O=NaHCO3+NH4Cl;(4)Na2CO3+SiO2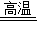 Na2SiO3+CO2↑;CaCO3+SiO2
Na2SiO3+CO2↑;CaCO3+SiO2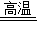 CaSiO3+CO2↑;(5)Fe2O3+6HCl=2FeCl3+3H2O;(6)制备氢气消耗电能大,成本高;(7)铵态氮肥与碱发生反应放出氨气,肥效降低.
CaSiO3+CO2↑;(5)Fe2O3+6HCl=2FeCl3+3H2O;(6)制备氢气消耗电能大,成本高;(7)铵态氮肥与碱发生反应放出氨气,肥效降低.点评:本题考查利用课本知识解决新问题能力,能加深学生对课本知识的理解,训练学生的思维能力.

练习册系列答案
相关题目