题目内容
下列物质含有不同原子团的是
- A.CaCO3Na2CO3
- B.KNO3AgNO3
- C.KMnO4K2MnO4
- D.CuSO4PbSO4
C
分析:根据的原子团组成分析,相同的原子团,应是组成元素、原子个数、原子团在化合物中显示的化合价都相同,否则就不是相同的原子团.
解答:A、CaCO3 Na2CO3中的都含有碳酸根,都是-2价,化合价相同,所以,A不符合题意;
B、KNO3 AgNO3中的都含有硝酸根,都是-1价,化合价相同;所以,B不符合题意;
C、KMnO4中的原子团为MnO4,是高锰酸根,在化合物中的化合价为-1价,而K2MnO4中的原子团为MnO4,是锰酸根,在化合物中的化合价为-2价,显然种类不同,故C正确;
B、CuSO4 PbSO4的原子团都是SO4,是硫酸根,在化合物中的化合价都是-2价,种类相同,故D不符合题意;
故选C.
点评:本题考查学生对于化合物中原子团的认识,不能只从表面上原子的个数和元素的种类作判断,还要从原子团的化合价进行判断.
分析:根据的原子团组成分析,相同的原子团,应是组成元素、原子个数、原子团在化合物中显示的化合价都相同,否则就不是相同的原子团.
解答:A、CaCO3 Na2CO3中的都含有碳酸根,都是-2价,化合价相同,所以,A不符合题意;
B、KNO3 AgNO3中的都含有硝酸根,都是-1价,化合价相同;所以,B不符合题意;
C、KMnO4中的原子团为MnO4,是高锰酸根,在化合物中的化合价为-1价,而K2MnO4中的原子团为MnO4,是锰酸根,在化合物中的化合价为-2价,显然种类不同,故C正确;
B、CuSO4 PbSO4的原子团都是SO4,是硫酸根,在化合物中的化合价都是-2价,种类相同,故D不符合题意;
故选C.
点评:本题考查学生对于化合物中原子团的认识,不能只从表面上原子的个数和元素的种类作判断,还要从原子团的化合价进行判断.

练习册系列答案
相关题目
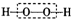 ②H-O-H
②H-O-H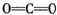 ④
④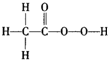
 和
和 代表两种不同元素的原子.这两种元素分别组成的单质在点燃条件下发生反应,反应前后的微观模拟图如下图所示,请回答下列问题.
代表两种不同元素的原子.这两种元素分别组成的单质在点燃条件下发生反应,反应前后的微观模拟图如下图所示,请回答下列问题. 、B代表
、B代表 ,请用A、B表示该反应
,请用A、B表示该反应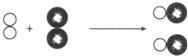 的化学方程式:
的化学方程式: