题目内容
【题目】实验室常用下图所示装置测定空气中氧气含量. 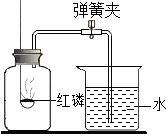
(1)若有1.24g红磷发生反应,则根据化学方程式计算,产生的固体(P2O5)有多少克?
(2)该试验中红磷过量,你认为是否有道理?(填“是”或“否”),你的理由是 .
(3)在动手实验的过程中,你认为该实验的不足是(至少一条)
【答案】
(1)解:设产生固体的质量为X
4P+5O2 | 2P2O5 |
124 | 284 |
1.24g | x |
![]()
解得:X═2.84g
答:产生固体的质量为2.84g
(2)是;红磷过量,尽可能将集气瓶中的氧气消耗完
(3)红磷被点燃后缓慢伸入集气瓶内,致使部分空气因热膨胀而逸出集气瓶(或磷在空气中燃烧会污染空气或导气管内存有空气会使实验误差较大)
【解析】解:(2)该实验的原理是消耗氧气,使装置内外产生压强差,为了使氧气全部耗尽,因此红磷要过量. 所以答案是:是; 红磷过量,尽可能将集气瓶中的氧气消耗完.(3)该实验注意点很多,排除药品量和装置气密性的影响外,还可从环保、操作等方面考虑.从操作角度看不足为:红磷被点燃后缓慢伸入集气瓶内,致使部分空气因热膨胀而逸出集气瓶;从环保角度考虑不足为:磷在空气中燃烧会污染空气;从利用的装置看导气管内存有空气会使实验误差较大.
所以答案是:红磷被点燃后缓慢伸入集气瓶内,致使部分空气因热膨胀而逸出集气瓶(或磷在空气中燃烧会污染空气或导气管内存有空气会使实验误差较大).
【考点精析】关于本题考查的根据化学反应方程式的计算,需要了解各物质间质量比=系数×相对分子质量之比才能得出正确答案.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目