题目内容
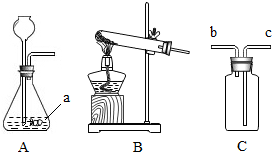 某学习小组围绕“气体实验室制取”进行了研讨.请你参与完成下面的问题.
某学习小组围绕“气体实验室制取”进行了研讨.请你参与完成下面的问题.(1)实验室制取CO2的化学方程式为
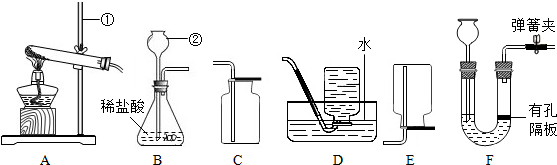
(2)图A装置中仪器a的名称是
(3)收集有毒气体SO2时,常采用图C收集装置,气体应从
考点:二氧化碳的实验室制法,书写化学方程式、文字表达式、电离方程式
专题:常见气体的实验室制法、检验、干燥与净化
分析:实验室制取CO2,是在常温下,用碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,H2SO4与CaCO3反应生成CaSO4,CaSO4微溶于水,附着在CaCO3的表面,阻止反应进一步发生;锥形瓶是常用的反应容器,实验室常用无水醋酸钠固体与碱石灰在加热的情况下制CH4,因此需要加热;收集有毒气体SO2时,常采用C收集装置,气体应从长管进入,因为二氧化硫的密度比空气的密度大;
解答:解:(1)碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,配平即可,故答案为:CaCO3+2HCl=CaCl2+H2O+CO2↑;
H2SO4与CaCO3反应生成CaSO4,CaSO4微溶于水,附着在CaCO3的表面,阻止反应进一步发生;
(2)锥形瓶是常用的反应容器,实验室常用无水醋酸钠固体与碱石灰在加热的情况下制CH4,因此属于固体加热型装置;故答案为:锥形瓶;B;
(3)收集有毒气体SO2时,常采用③收集装置,气体应从长管进入,因为二氧化硫的密度比空气的密度大;故答案为:c;
故答案为:(1)CaCO3+2HCl=CaCl2+H2O+CO2↑;H2SO4与CaCO3反应生成CaSO4,CaSO4微溶于水,附着在CaCO3的表面,阻止反应进一步发生;
(2)锥形瓶;B
(3)c
H2SO4与CaCO3反应生成CaSO4,CaSO4微溶于水,附着在CaCO3的表面,阻止反应进一步发生;
(2)锥形瓶是常用的反应容器,实验室常用无水醋酸钠固体与碱石灰在加热的情况下制CH4,因此属于固体加热型装置;故答案为:锥形瓶;B;
(3)收集有毒气体SO2时,常采用③收集装置,气体应从长管进入,因为二氧化硫的密度比空气的密度大;故答案为:c;
故答案为:(1)CaCO3+2HCl=CaCl2+H2O+CO2↑;H2SO4与CaCO3反应生成CaSO4,CaSO4微溶于水,附着在CaCO3的表面,阻止反应进一步发生;
(2)锥形瓶;B
(3)c
点评:本考点主要考查了仪器的名称、气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.

练习册系列答案
相关题目
在地壳中含量最多的金属元素和非金属元素组成的化合物的化学式是( )
| A、Al2O3 |
| B、FeO |
| C、Fe2O3 |
| D、SiO2 |
我们生活在多姿多彩的物质世界里,下列变化中没有新物质生成的是( )
| A、冰雪消融 |
| B、葡萄酿成酒 |
| C、用食醋除去暖水瓶中的水垢 |
| D、铜器锈蚀变绿 |
实验规律操作是获得实验成功的重要保证,如图所示实验操作中,正确的是( )
A、 |
B、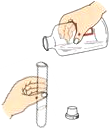 |
C、 |
D、 |
向水中加入下列物质,水的温度明显下降的是( )
| A、CaO |
| B、NaOH |
| C、浓硫酸 |
| D、NH4NO3 |