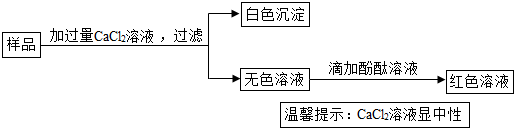
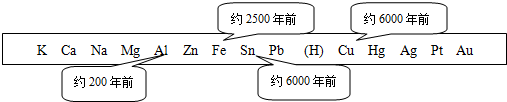
题目内容
兴趣小组的同学从实验室中收集一桶含有FeSO4、CuSO4的废液.他们想从中回收金属铜和硫酸亚铁晶体,设计了如下方案:

(1)操作a、b的名称是 .步骤Ⅱ中发生反应的化学方程式为 .
(2)甲同学提出X可用金属铁,乙同学认为X可用金属锌,你认为谁的意见是正确的,理由是 .加入过量的金属X的目的是 .

(1)操作a、b的名称是
(2)甲同学提出X可用金属铁,乙同学认为X可用金属锌,你认为谁的意见是正确的,理由是
考点:金属的化学性质,过滤的原理、方法及其应用,书写化学方程式、文字表达式、电离方程式
专题:金属与金属材料
分析:(1)过滤是分离不溶性杂质的方法,根据反应原理写出反应化学方程式.
(2)根据实验目的是要除去硫酸亚铁中硫酸铜杂质,在除杂时要注意“除去杂质,不引入新的杂质”的原则分析.
(2)根据实验目的是要除去硫酸亚铁中硫酸铜杂质,在除杂时要注意“除去杂质,不引入新的杂质”的原则分析.
解答:解:(1)过滤是分离不溶性杂质的方法,因此其目的是除去溶液中难溶性的杂质,步骤Ⅱ是将铁和铜分离,稀硫酸和铁反应产生硫酸亚铁和氢气,反应的方程式为:Fe+H2SO4=FeSO4+H2↑;
(2)根据活泼金属可以将不活泼金属溶液中置换出来,铁和锌都能除去硫酸亚铁中硫酸铜杂质,但除杂时要注意“除去杂质,不引入新的杂质”的原则,因此应该加入铁,不会引人新的杂质;加入过量的金属X的目的是把铜全部置换出来或得到全部的铜.
故答案为:(1)过滤;Fe+H2SO4=FeSO4+H2↑;
(2)甲正确,因为锌会把铁、铜都置换出来,引入杂质硫酸锌晶体;把铜全部置换出来或得到全部的铜.
(2)根据活泼金属可以将不活泼金属溶液中置换出来,铁和锌都能除去硫酸亚铁中硫酸铜杂质,但除杂时要注意“除去杂质,不引入新的杂质”的原则,因此应该加入铁,不会引人新的杂质;加入过量的金属X的目的是把铜全部置换出来或得到全部的铜.
故答案为:(1)过滤;Fe+H2SO4=FeSO4+H2↑;
(2)甲正确,因为锌会把铁、铜都置换出来,引入杂质硫酸锌晶体;把铜全部置换出来或得到全部的铜.
点评:本题主要考查了金属活动性顺序表的应用,难度不大,熟记金属活动性顺表、理解其应用是解答本题的关键,另外还要熟知除杂的原则及化学方程式的书写.

练习册系列答案
 轻巧夺冠周测月考直通中考系列答案
轻巧夺冠周测月考直通中考系列答案
相关题目
下列化学方程式的书写对应的部分实验现象,均正确的是( )
A、4P+5O2
| ||||
B、Mg+O2
| ||||
C、4Fe+3O2
| ||||
D、C2H5OH+2O2
|
判断一个变化是否是化学变化的依据是( )
| A、看是否有沉淀生成 |
| B、看是否有气体放出 |
| C、看在变化中是否放热 |
| D、看在变化过程中是否有新物质生成 |
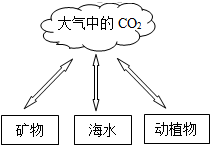 我市正在逐步将管道煤气由石油液化气(主要成分是丁烷)改为天然气,小明家要进行灶具和燃气泄漏报警器的调整.请填空:
我市正在逐步将管道煤气由石油液化气(主要成分是丁烷)改为天然气,小明家要进行灶具和燃气泄漏报警器的调整.请填空: