题目内容
【题目】以下是日常生活中常用各种清洗剂。

(1)使用洗涤灵清洗餐具上的油污,这是因为它具有 功能;
(2)清除以下物质,可使用炉具清洁剂的是 (填字母序号);
A.铁锈 B.油污 C.水垢
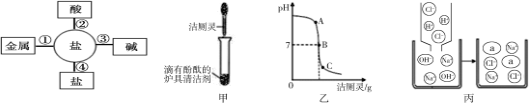
(3)“污渍爆炸盐”溶于水后会生成Na2CO3和H2O2。将爆炸盐溶于水后,再加入足量的洁厕灵,产生能使澄清石灰水变浑浊的气体,此反应体现了上图中 (选填①②③④)盐的性质关系;
(4)将洁厕灵滴入炉具清洁剂中,如上图甲所示。
①若反应后溶液呈红色,则反应后溶液中的溶质是(酚酞除外) ,此时溶液可用图乙中 (选填A、B、C)点处表示;
②若反应后溶液pH为7,图丙中a微粒的化学式为 ;
③丙中反应没有明显现象,为证明反应发生,可加入的试剂有 。
A.无色酚酞溶液 B.石灰石 C.硝酸银溶液 D.锌粒
【答案】(1)乳化 (2)B (3)② (4)①NaCl、NaOH A ②H2O ③A B D
【解析】
试题分析:(1)我们使用洗涤灵清洗餐具上的油污,这是因为它具有乳化功能;(2)因为洁厕灵中含有盐酸,故可与盐酸反应得为铁锈、水垢;(3)“污渍爆炸盐”溶于水后会生成Na2CO3和H2O2。将爆炸盐溶于水后,再加入足量的洁厕灵,产生能使澄清石灰水变浑浊的气体,这一反应了体现右图中盐与酸反应;(4)①若反应后溶液呈红色,说明溶液呈碱性,则反应后溶液中的溶质是(酚酞除外)NaCl NaOH;此时溶液可用图乙中A点表示;②若反应后溶液pH为7,图丙中a微粒的化学式为H2O,③丙中反应没有明显现象,为证明反应发生,可加入的试剂有A B D

【题目】同学们用Na2CO3溶液和浓HCl来研究简易灭火器的反应原理时,对废液的成分进行研究。
(1)写出上述化学方程式 ,反应后溶液中一定有 。对可能含有的物质进行探究。
(2)确定废液中是否含有盐酸:
①选用如图所示物质X是酸碱指示剂中的 溶液。

②向废液中加入少量的镁粉,观察到 ,确定废液中一定没有盐酸。
(3)确定废液中是否含有Na2CO3,可选用 测出废液的pH=10,确定废液中一定含有Na2CO3。
(4)欲从废液中得到纯净的NaCl,请完成如下实验方案设计。
方案 | 加入试剂 | 分离方法 | 方案评价 |
一 | 适量Ca(NO3)2 | 过滤、蒸发结晶 | 不可行,理由是 |
二 | 稍过量的 | 可行 |
(5)按如下图方案分离BaCl2和NaCl的固体混合物时,X溶液中溶质是 。


