题目内容
【题目】现有H、C、O、S、N、Cu、Ca七种元素,请从中选择适当的元素组成符合要求的物质,并按要求填空。
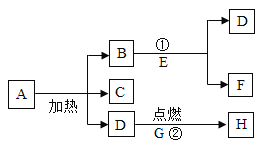
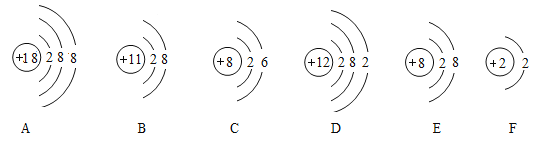
(1)A为碳不充分燃烧的生成物,写出A物质的化学式:_____。
(2)B为最简单的有机物,写出B物质在空气中燃烧的化学方程式:_____。
(3)C为实验室常用燃料,写出C物质的化学式:_____,C物质还可以通过淀粉类粮食发酵制得,淀粉的化学式_____。
(4)D为澄清石灰水的溶质,标出D物质中显正价元素的化合价:_____。
(5)E的水溶液为蓝色,且工业上常用E和D配制波尔多液,写出配制波尔多液的化学反应方程式_____;E中阴离子的离子符号为_____。
(6)F为一种常见的化肥,若与D混用,会产生_____(填化学式)降低肥效。
【答案】CO CH4+2O2![]() CO2+2H2O C2H5OH (C6H10O5)n
CO2+2H2O C2H5OH (C6H10O5)n ![]() Ca(OH)2+CuSO4=Cu(OH)2↓+CaSO4 SO42- NH3
Ca(OH)2+CuSO4=Cu(OH)2↓+CaSO4 SO42- NH3
【解析】
解:(1)碳不充分燃烧生成一氧化碳;化学式为:CO;
(2)甲烷是结构最简单的有机物,在空气中燃烧生成二氧化碳和水;化学方程式为:CH4+2O2![]() CO2+2H2O;
CO2+2H2O;
(3)酒精是实验室中最常用的燃料,其化学式为C2H5OH;淀粉的化学式为(C6H10O5)n;
(4)氢氧化钙是石灰水的溶质,其中钙元素显+2价,氢元素显+1价,氧元素显—2价,化合价标注在元素符号的正上方,正负号在前,数值在后;可表示为:![]() ;
;
(5)硫酸铜溶液是蓝色的,D是氢氧化钙,硫酸铜与氢氧化钙反应生成氢氧化铜蓝色沉淀和硫酸钙,化学反应方程式为:Ca(OH)2+CuSO4=Cu(OH)2↓+CaSO4;硫酸铜中的阴离子是硫酸根离子,符号为:SO42-;
(6)D是氢氧化钙,由提供的元素组成的硝酸铵、碳酸氢铵均属于铵态氮肥,铵态氮肥与氢氧化钙反应能释放出氨气,造成肥效降低。

 优加精卷系列答案
优加精卷系列答案【题目】材料是人类赖以生存和发展的重要物质,目前使用量最多的金属材料仍然是钢铁。
(一)实验室用赤铁矿模拟工业炼铁的化学方程式为_____,炼得的铁是_____(填“单质铁”或“合金”),该反应_____(填“是”或“不是”)置换反应。
(二)FeCO3是菱铁矿的主要成分,具有还原性,在空气中灼烧生成铁的氧化物和CO2气体。要探究碳酸亚铁和氧气充分反应后的固体成分,请你参与小华同学的探究:
(查阅资料)
① FeO是一种黑色粉末,它不稳定,在空气中加热,就迅速被氧化成四氧化三铁,四氧化三铁能与盐酸反应生成氯化亚铁、氯化铁和水。
②FeCl2能使高锰酸钾溶液褪色,而FeCl3不能;FeCl3溶液中滴加KSCN溶液,溶液变红色,FeCl2溶液中滴加KSCN溶液,溶液不出现红色。
(猜想与假设)
猜想1:固体成分是氧化铁;
猜想2:固体成分是四氧化三铁;
猜想3:_____。
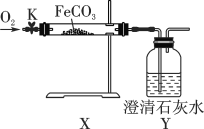
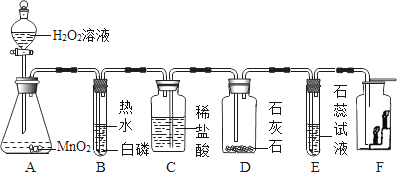
(活动与探究)连接仪器、装好药品如图所示(加热和固定装置已省略),打开止水夹K,通入氧气,加热玻璃管X。当Y瓶中产生的沉淀不再增加时,停止加热,继续通入氧气至玻璃管冷却。取玻璃管里的少量固体于试管中,滴加盐酸,微热,固体完全溶解。将所得溶液分成甲、乙两份进行实验。
实验编号 | 实验步骤 | 实验现象 |
a | 向甲溶液中滴加KSCN溶液 | 溶液变红色 |
b | 向乙溶液中滴加酸性高锰酸钾溶液 | 高锰酸钾溶液的紫红色不消失 |
(结论与反思)
(1)由上述实验现象可知,FeCO3在氧气中高温灼烧得到的固体产物是_____,因此,猜想_____(填“1”“2”或“3”)是正确的。
(2)FeCO3在氧气中高温灼烧的化学方程式为_____。
(3)上述实验_____(填“a”或“b”)是多余的,因为_____。
(总结与提升)
(1)若实验结束时观察到Y瓶中仍然是澄清的,可能的原因是澄清石灰水的量不足,导致生成的碳酸钙转变成了可溶于水的碳酸氢钙。碳酸氢钙的化学式为_____。
(2)CO2使澄清石灰水变浑浊的化学方程式为_____。
(3)华雪同学经过反思,觉得该实验设计还存在问题,因为如果在实验b中观察到_____,就不能确定哪个猜想是正确的。所以小华同学又对该实验进行了定量探究:取11.6 g纯净的碳酸亚铁固体,在空气中高温灼烧至恒重,称得固体质量净减3.6 g。通过计算即可确定:FeCO3和氧气充分反应后的固体成分是_____。