题目内容
一定质量的氯化铜和40g盐酸组成的混合溶液中慢慢

滴入20%的氢氧化钠溶液并振荡,所加氢氧化钠溶液
的质量与生成沉淀的质量的关系如图所示,下列判断
中正确的是

滴入20%的氢氧化钠溶液并振荡,所加氢氧化钠溶液
的质量与生成沉淀的质量的关系如图所示,下列判断
中正确的是
| A.最终生成沉淀的质量为14.7g |
| B.40g盐酸的溶质的质量分数是27.375% |
| C.生成沉淀的质量随氢氧化钠溶液的滴加而逐渐增多 |
| D.当加入的氢氧化钠溶液为60g时,所得溶液为氯化钠溶液 |
D
分析:在有酸存在的情况下,碱总是先与酸反应,等把酸完全消耗掉之后才与其它物质发生反应,所以本题中所发生反应的先后顺序为:(1)NaOH+HCl═NaCl+H2O,(2)CuCl2+2NaOH═Cu(OH)2↓+2NaCl 从图中可以分析出第一个反应所消耗的氢氧化钠溶液的质量为20g,第二个反应所消耗的氢氧化钠溶液的质量为40g.
解:A设生成沉淀的质量为x,则:
CuCl2+2NaOH═Cu(OH)2↓+2NaCl
80 98n
40g x20%=8g x
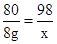
解得:x=9.8g
故A错.
B 设盐酸的质量分数为y,则:
NaOH+HCl═NaCl+H2O
40 36.5
20gx20% 40g?y
=4g

解得:y=9.125%
故B错.
C选项说的不严密,一开始加入氢氧化钠溶液不会产生沉淀,到最后把氯化铜消耗完之后,也不会再产生沉淀故 C错
D由上分析中所发生的两个化学反应及图可知,加入60g氢氧化钠溶液时,恰好把氯化铜和盐酸消耗掉,所以最后所得溶液中的溶质只有氯化钠也就是氯化钠溶液,故D正确.
故选D
解:A设生成沉淀的质量为x,则:
CuCl2+2NaOH═Cu(OH)2↓+2NaCl
80 98n
40g x20%=8g x
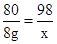
解得:x=9.8g
故A错.
B 设盐酸的质量分数为y,则:
NaOH+HCl═NaCl+H2O
40 36.5
20gx20% 40g?y
=4g

解得:y=9.125%
故B错.
C选项说的不严密,一开始加入氢氧化钠溶液不会产生沉淀,到最后把氯化铜消耗完之后,也不会再产生沉淀故 C错
D由上分析中所发生的两个化学反应及图可知,加入60g氢氧化钠溶液时,恰好把氯化铜和盐酸消耗掉,所以最后所得溶液中的溶质只有氯化钠也就是氯化钠溶液,故D正确.
故选D

练习册系列答案
相关题目
