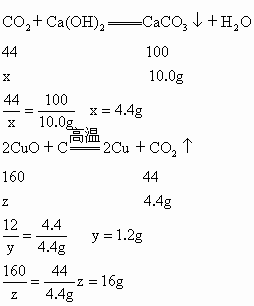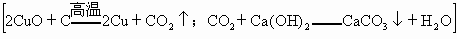题目内容
现有
21.2g组成的黑色固体混合物,放入试管中,高温加热,使其充分反应后,把生成的气体全部通入足量的澄清石灰水中,结果生成10.0g白色沉淀.求黑色固体混合物中碳与氧化铜的质量分数.(计算结果精确到0.1%)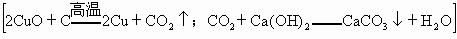
答案:24.5%,75.5%$5.7%,94.3%
解析:
解析:
|
解:设生成 10.0g白色沉淀需要 质量为x,参加反应的C质量为y,参加反应的CuO质量为z. 质量为x,参加反应的C质量为y,参加反应的CuO质量为z.
因为 1.2g+16g=17.2g<21.2g,故有4g固体剩余.①当剩余 4g固体为碳时:氧化铜的质量分数为: 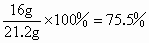
碳的质量分数为: 1-75.5%=24.5%②当剩余 4g固体为氧化铜时:碳的质量分数为: 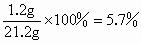
氧化铜的质量分数为: 1-5.7%=94.3%答: C和CuO的质量分数分别为24.5%和75.5%或5.7%和94.3%.此题需讨论,解答的关键在于通过产生的 10.0g 计算出CuO与C反应产生 计算出CuO与C反应产生 的质量后,以 的质量后,以 的质量算出参加反应的CuO和C的质量,然后再分CuO或C过量两种情况讨论. 的质量算出参加反应的CuO和C的质量,然后再分CuO或C过量两种情况讨论. |

练习册系列答案
 特高级教师点拨系列答案
特高级教师点拨系列答案
相关题目