题目内容
【题目】“化学用语”是学习化学的重要工具,按要求填空
(1)写出对应的化学符号
①氯气_________________________;
②两个锌离子_________________________;
③ 3个铁离子_________________________;
④氯化铝__________________________;
⑤硝酸铵__________________________;
⑥空气中含量最多的气体__________________________;
⑦硫酸__________________________;
⑧氧化钙中钙的化合价为+2价__________________________;
⑨构成氦气的微粒_________________________;
⑩硅的原子结构示意图__________________________。
(2)写出下列反应的符号表达式
①硫在氧气中燃烧: _________________________;
②汞在空气中加热: _________________________;
③电解水: _________________________;
④铁在氧气中燃烧: _________________________。
【答案】Cl2 2Zn2+ 3Fe3+ AlCl3 NH4NO3 N2 H2SO4 ![]() He
He  S+O2
S+O2![]() SO2 Hg+O2
SO2 Hg+O2![]() HgO H2O
HgO H2O![]() H2+ O2 Fe+O2
H2+ O2 Fe+O2![]() Fe3O4
Fe3O4
【解析】
(1)氯气是由氯分子构成,每个氯分子是由两个氯原子构成,氯气的化学式为:Cl2,故填写:Cl2;
先写微粒个数“2”,再写锌离子(先写锌元素,再写电量“2”,最后写电性“+”),故填写:2Zn2+;
先写微粒个数“3”,再写铁离子(先写铁元素,再写电量“3”,最后写电性“+”),故填写:3Fe3+;
氯化铝的化学式为:AlCl3,故填写:AlCl3;
硝酸铵的化学式为:NH4NO3,故填写:NH4NO3;
空气中含量最多的气体是氮气,故填写:N2;
硫酸的化学式为:H2SO4,故填写:H2SO4;
先写氧化钙的化学式,在钙元素的正上放标出化合价(先写价态“+”,再写价数“2”),故填写:![]() ;
;
氦气是由氦原子构成,故填写:He;
硅原子的质子数为14,核外电子数为14,电子排布方式为:2,8,4,故填写: ;
;
(2)硫在氧气中燃烧生成二氧化硫,故填写:S+O2![]() SO2;
SO2;
汞在空气中加热生成氧化汞,故填写:Hg+O2![]() HgO;
HgO;
电解水生成氢气和氧气,故填写:H2O![]() H2+ O2;
H2+ O2;
铁在氧气中燃烧生成四氧化三铁,故填写:Fe+O2![]() Fe3O4。
Fe3O4。

 轻松夺冠全能掌控卷系列答案
轻松夺冠全能掌控卷系列答案【题目】某化学课堂围绕“酸碱中和反应”,将学生分成若干小组开展探究活动,请你和他们仪器完成以下实验探究。
(1)(演示实验)将一定量稀盐酸加入到盛氢氧化钙溶液的小烧杯中,该反应的化学方程式是_____________(查阅资料)CaCl2溶液显中性
(提出问题)实验中未观察到明显显像,部分同学产生了疑问:反应后溶液中溶质的成分是什么?
(2)(猜想与假设)针对疑问,甲组同学猜想如下:
猜想Ⅰ:只有CaCl2 猜想Ⅱ:有_____________;猜想Ⅲ:有CaCl2和Ca(OH)2;猜想Ⅳ:有CaCl2、HCl和Ca(OH)2
(3)乙组同学对以上猜想提出质疑,认为猜想Ⅳ不合理,其理由是_______________
(4)(实验探究)为了验证其余猜想,各小组进行了下列三个方案的探究。
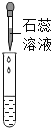
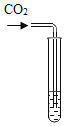
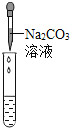
实验方案 | 滴加紫色石蕊溶液 | 通入 | 滴加 |
实验操作 |
|
|
|
实验现象 | ________________ | ________________ | 产生白色沉淀 |
实验结论 | 溶液中含有Ca(OH)2 | 溶液中含有Ca(OH)2 | 溶液中含有Ca(OH)2 |
(得出结论)通过探究,全班同学一致确定猜想Ⅲ是正确的。
(5)(评价反思)丙组同学认为滴加Na2CO3溶液产生白色沉淀,并不能证明溶液中一定含有Ca(OH)2,请你帮助他们说明原因_______________________________
(6)在分析反应后所得溶液中溶质的成分时,除了考虑生成物外,还需要考虑______________
(7)若用200克稀盐酸和12克石灰石(杂质不溶于水也不溶于酸)反应制取二氧化碳气体为4.4克,则该石灰石中CaCO3质量分数是多少?________________________