题目内容
【题目】(1)2008年“三鹿奶粉事件”的“元凶”是三聚氰胺,其化学式为C3H6N6。三聚氰胺常被用作化工原料,微溶于水,有轻微毒性。三聚氰胺的相对分子质量是________________,碳、氢、氮三元素的质量比为___________,因三聚氰胺的含氮量较高,所以被不法分子添加到奶制品中,以“提高”蛋白质含量。37.8克三聚氰胺中氮元素质量为______克。
(2)水是生命之源、万物之基,是人类宝贵的自然资源,我们每个人都要关心水、爱护水、节约用水。
①我国规定生活饮用水的水质必须达到下述四项指标:a 不得呈现异色 b 不得有异味 c 应澄清透明d 不得含有细菌和病毒。其中“c指标”可以通过 ____________________操作达到;
②某校化学兴趣小组同学发现,长期使用的热水壶底部有一层水垢,水垢的主要成分是碳酸钙和氢氧化镁。为了测定水垢中碳酸钙的含量,他们将足量质量分数为10%的盐酸加入到10.4g水垢中,产生CO2气体的情况如下图所示。

从图中可以看出,水垢与盐酸完全反应后生成的二氧化碳的质量为______克,水垢中碳酸钙的质量分数是___。若水垢中只含碳酸钙和氢氧化镁,则完全反应后消耗盐酸的质量为___克。
【答案】126 6︰1︰14 25.2 过滤 3.3 72.1% 91.25
【解析】
(1)根据三聚氰胺的化学式C3H6N6,三聚氰胺的相对分子质量=12×3+1×6+14×6=126;其中碳、氢、氮的元素质量比=(12×3):(1×6):(14×6)=6:1:14;37.8克三聚氰胺中氮元素质量![]() 。故填:126;6:1:14;25.2
。故填:126;6:1:14;25.2
(2)①其中“c指标”可以通过过滤操作达到。故填:过滤
②从图中可看出生成的二氧化碳最多是3.3g。设碳酸钙的质量为x。和碳酸钙反应的盐酸溶液中溶质的质量为y。
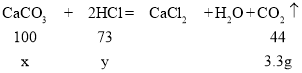
![]()
x=7.5g,y=5.475g;水垢中碳酸钙的质量分数=![]()
答:水垢中碳酸钙的质量分数为72.1%。
氢氧化镁的质量=10.4g-7.5g=2.9g设和氢氧化镁反应的盐酸溶液中溶质的质量为z。
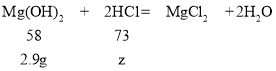
![]()
z=3.65g
所需盐酸溶液的质量为![]() ;
;
答:至少需要质量分数为10%的盐酸的质量是91.25g。故填:3.3;72.1%;91.25

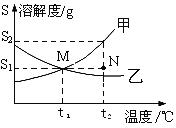
【题目】硝酸钾和氯化钠在不同温度下的溶解度如下表,请回答。
温度/℃ | 20 | 40 | 60 | 80 | 100 | |
溶解度/g | 硝酸钾 | 31.6 | 63.9 | 110 | 169 | 246 |
氯化钠 | 36.0 | 36.6 | 37.3 | 38.4 | 39.8 | |
(1)60℃时硝酸钾的溶解度是_____g。
(2)若硝酸钾中混有少量的氯化钠,提纯硝酸钾可以采取的方法是_____。
(3)20℃时,将硝酸钾和氯化钠两种固体各36g分别加入盛有100水的烧杯中,充分溶解后可观察到如图所示的现象。
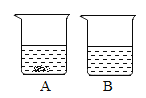
①烧杯A中溶解的物质是_____。
②若向烧杯A中加入一定量的水使剩余固体刚好全部溶解变为饱和溶液,则溶液中溶质的质量分数_____(填“变大”、“变小”或“不变”)。
③若将A、B烧杯中的物质同时升温至80℃,则A、B中溶质的质量_____(填“一定”或“不一定”)相等。
【题目】某矿石主要成分是MgO,含少量的Fe2O3、CuO和SiO2杂质。用该矿石制备Mg(OH)2的工艺流程简图如图:
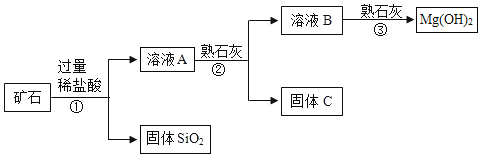
回答下列问题:
(1)步骤①和步骤②均用到的操作是_____。
(2)溶液A中所含的阳离子有Fe3+、Cu2+、Mg2+和_____(填离子符号)。
(3)已知部分金属阳离子以氢氧化物形成沉淀时溶液的pH见下表:
对应离子 | Fe3+ | Cu2+ | Mg2+ |
开始沉淀时的pH | 1.9 | 4.2 | 9.1 |
完全沉淀时的pH | 3.2 | 6.7 | 11.1 |
步骤②加入熟石灰,调节溶液的pH范围为_____,固体C中所含成分的化学式为_____。
(4)步骤③制得Mg(OH)2的化学方程式为_____。