题目内容
 某兴趣小组对氢氧化钠固体暴露在空气中的变质情况进行了研究.把一小块固体氢氧化钠放在表面皿里,长时间暴露在空气中,发现其固体表面逐渐湿润,部分溶化成液体后又逐渐形成晶体,最终变成粉末.请回答兴趣小组产生的下列问题:
某兴趣小组对氢氧化钠固体暴露在空气中的变质情况进行了研究.把一小块固体氢氧化钠放在表面皿里,长时间暴露在空气中,发现其固体表面逐渐湿润,部分溶化成液体后又逐渐形成晶体,最终变成粉末.请回答兴趣小组产生的下列问题:(1)实验室中,氢氧化钠固体应怎样保存?
(2)氢氧化钠固体暴露在空气中,表面容易变湿,主要原因是什么?
(3)氢氧化钠固体长期暴露在空气中,最终产物主要是什么
(4)用酚酞试液
(5)检验氢氧化钠固体已经变质加入
(6)为了检验氢氧化钠是否已经全部变质,兴趣小组中小薇同学设计了如下实验方案:准确称取一定质量的变质固体样品,放在如图所示装置中,然后从分液漏斗中加入足量的盐酸,用排水法收集产生的二氧化碳,根据二氧化碳的体积和密度计算变质产物的质量,确定是否全部变质.
①你认为这个方案
考点:药品是否变质的探究,常见碱的特性和用途,碱的化学性质,盐的化学性质,书写化学方程式、文字表达式、电离方程式
专题:科学探究
分析:(1)根据氢氧化钠露置与空气中会吸收水分而潮解,然后和二氧化碳反应进行分析;
(2)根据氢氧化钠露置与空气中会吸收水分而潮解进行分析;
(3)根据氢氧化钠变质是和空气中的二氧化碳反应生成了碳酸钠进行分析;
(4)根据变质之后的产物碳酸钠的溶液呈碱性,能使酚酞变红进行分析;
(5)根据可溶性碳酸盐的性质进行分析;
(6)根据二氧化碳能溶于水,不能使用排水法收集进行分析.
(2)根据氢氧化钠露置与空气中会吸收水分而潮解进行分析;
(3)根据氢氧化钠变质是和空气中的二氧化碳反应生成了碳酸钠进行分析;
(4)根据变质之后的产物碳酸钠的溶液呈碱性,能使酚酞变红进行分析;
(5)根据可溶性碳酸盐的性质进行分析;
(6)根据二氧化碳能溶于水,不能使用排水法收集进行分析.
解答:解:(1)氢氧化钠固体露置于空气中容易变质,所以实验室中,氢氧化钠固体必须密封保存;
(2)氢氧化钠以吸收空气中的水分而潮解,从而使表面变得潮湿,主要原因是:氢氧化钠固体吸收水或潮解;
(3)氢氧化钠潮解之后会和空气中的二氧化碳反应生成碳酸钠,所以最终产物是:碳酸钠;
(4)氢氧化钠溶液呈碱性,同时变质之后的碳酸钠溶液也呈碱性,所以不能根据酚酞是否变红来检验氢氧化钠是否变质,原因是:碳酸钠溶液也能使酚酞试液变红;
(5)要检验氢氧化钠是否变质,就是检验碳酸盐的存在,可以使用盐酸检验,盐酸和碳酸钠反应生成氯化钠、水和二氧化碳,化学方程式为:Na2CO3+2HCl=2NaCl+H2O+CO2↑;
(6)CO2能溶于水不能用排水法集气,否则会导致计算的结果不准确,所以这个方案不行,理由是:CO2能溶于水不能用排水法集气,用排水法收集误差较大.
故答案为:(1)密封保存;
(2)氢氧化钠固体吸收水或潮解;
(3)碳酸钠;
(4)不能,碳酸钠溶液也能使酚酞试液变红;
(5)HCl,Na2CO3+2HCl=2NaCl+H2O+CO2↑;
(6)不行,CO2能溶于水不能用排水法集气,用排水法收集误差较大.
(2)氢氧化钠以吸收空气中的水分而潮解,从而使表面变得潮湿,主要原因是:氢氧化钠固体吸收水或潮解;
(3)氢氧化钠潮解之后会和空气中的二氧化碳反应生成碳酸钠,所以最终产物是:碳酸钠;
(4)氢氧化钠溶液呈碱性,同时变质之后的碳酸钠溶液也呈碱性,所以不能根据酚酞是否变红来检验氢氧化钠是否变质,原因是:碳酸钠溶液也能使酚酞试液变红;
(5)要检验氢氧化钠是否变质,就是检验碳酸盐的存在,可以使用盐酸检验,盐酸和碳酸钠反应生成氯化钠、水和二氧化碳,化学方程式为:Na2CO3+2HCl=2NaCl+H2O+CO2↑;
(6)CO2能溶于水不能用排水法集气,否则会导致计算的结果不准确,所以这个方案不行,理由是:CO2能溶于水不能用排水法集气,用排水法收集误差较大.
故答案为:(1)密封保存;
(2)氢氧化钠固体吸收水或潮解;
(3)碳酸钠;
(4)不能,碳酸钠溶液也能使酚酞试液变红;
(5)HCl,Na2CO3+2HCl=2NaCl+H2O+CO2↑;
(6)不行,CO2能溶于水不能用排水法集气,用排水法收集误差较大.
点评:本题考查了氢氧化钠的性质以及碳酸盐的检验方法,完成此题,可以依据已有的知识结合题干叙述的内容进行.

练习册系列答案
相关题目
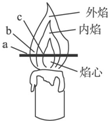 某同学对蜡烛(主要成分是石蜡)及其燃烧进行了如下探究.请填写下列空格:
某同学对蜡烛(主要成分是石蜡)及其燃烧进行了如下探究.请填写下列空格: 根据所给信息,回答下列问题
根据所给信息,回答下列问题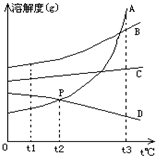 如图所示A、B、C、D为四种物质的溶解度曲线,请将正确答案填入空格内:
如图所示A、B、C、D为四种物质的溶解度曲线,请将正确答案填入空格内: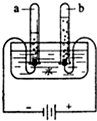 目前部分农村的饮用水主要还是地下水.饮用遭到污染或硬度大的地下水不利于人体健康.政府积极建设自来水厂,让农民喝上清洁的水.
目前部分农村的饮用水主要还是地下水.饮用遭到污染或硬度大的地下水不利于人体健康.政府积极建设自来水厂,让农民喝上清洁的水.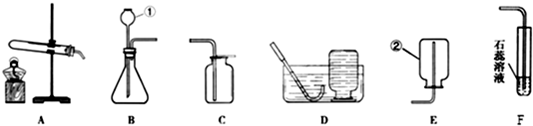
 联合国气候峰会主要讨论全球气候变化.请根据如图回答:
联合国气候峰会主要讨论全球气候变化.请根据如图回答: