题目内容
下列实验现象描述错误的是( )
| A.镁带在空气中燃烧发出耀眼的白光 |
| B.打开浓盐酸的瓶盖,瓶口出现白烟 |
| C.硫粉在氧气中燃烧,发出蓝紫色火焰 |
| D.电解水时正极产生的气体体积比负极产生的气体体积少 |
B
试题分析:A、镁带在空气中燃烧发出耀眼的白光,正确,B、浓盐酸具有挥发性,打开浓盐酸的瓶盖,瓶口出现白雾(盐酸小液滴),而不是白烟,错误,C、硫粉在氧气中燃烧,发出蓝紫色火焰,正确,D、电解水时正极产生的气体是氧气,负极产生的气体是氢气,氢气的体积时氧气体积的2倍,正确,故选B

练习册系列答案
相关题目
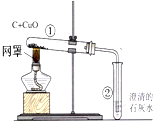

 CO2↑+CO↑+H2O)。用到的实验装置见下图:
CO2↑+CO↑+H2O)。用到的实验装置见下图: