题目内容
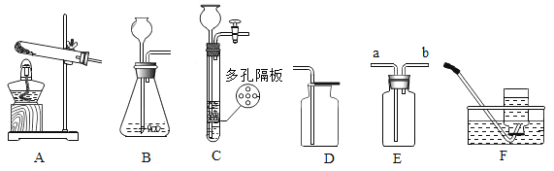
【题目】下图是配制溶质质量分数为10%的NaCl溶液的实验操作示意图:
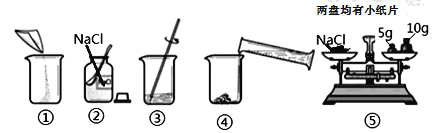
(1)用上图表示的序号表示配制溶液的正确操作顺序___________。
(2)图③中玻璃棒的作用是__________。
(3)称量NaCl时,天平平衡后的状态如图⑤所示,游码标尺示数如图,则称取NaCl的实际质量为______;若当时药品与砝码放反了,称取药品的质量变为__________。
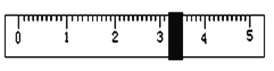
(4)根据计算需要量取水的体积是_____________mL(水的密度为1g/mL)。
【答案】②⑤①④③ 溶解时玻璃棒的作用是搅拌,加速固体溶解 18.2g 11.8g 163.8
【解析】
(1)根据用固体溶质氯化钠配制溶液的步骤:计算-称量-溶解,先取氯化钠进行称取,倒入烧杯;然后量取水,倒入盛氯化钠的烧杯中;最后进行溶解;
(2)溶解时玻璃棒的作用是搅拌,加速固体溶解;
(3)砝码的质量为10g+5g=15g,游码的质量为3.2g,所称取氯化钠的质量=15g+3.2g=18.2g;若当时药品与砝码放反了,称取药品的质量变为15g-3.2g=11.8g;
(4)所配制溶液的质量=![]() =182g,则需要水的质量=182g-18.2g=163.8g,合163.8mL;
=182g,则需要水的质量=182g-18.2g=163.8g,合163.8mL;
故答案为:(1)②⑤①④③;(2)溶解时玻璃棒的作用是搅拌,加速固体溶解;(3)18.2g;11.8g;(4)163.8mL。

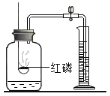
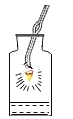
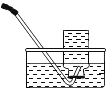
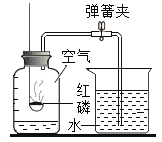
【题目】水在化学实验中有多种用途,对下列实验中水的作用解释不正确的是( )
A | B | C | D | |
实 验 装 置 |
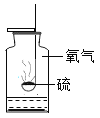
硫在氧气中燃烧 |
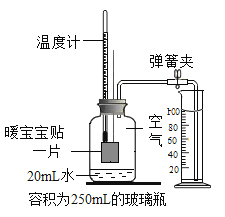
测定空气中氧气含量 |
铁丝在氧气中燃烧 |
排水法收集氧气 |
作用 | 集气瓶中的水; 吸收热量,防止集气瓶炸裂。 | 量筒中的水: 通过体积变化得出 空气中氧气的体积 | 集气瓶中的水: 冷却溅落熔融物, 防止集气瓶炸裂 | 集气瓶中先装满的水:先排尽瓶中空气并便于观察氧气何时集满。 |
A.AB.BC.CD.D