题目内容
【题目】根据下列装置图,回答问题:

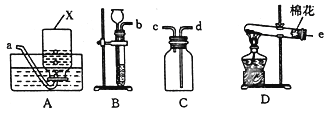
(1)写出仪器名称:①_________;②_________。
(2)实验室制取氢气,应选择发生装置是______________(填编号);若用排空气法收集,应选择收集装置是_________(填编号)。
(3)实验室用过氧化氢制取氧气的化学方程式:_____________。若用装置E收集氧气,实验结束时,移出导管,再_____________,取出集气瓶后,瓶口______________
(填“向上”或“向下”)放置于桌面。
(4)实验改进:查阅资料发现,氧化铜可用作过氧化氢分解制氧气的催化剂。现将一根绕成螺旋状的、表面已被氧化的铜丝组装成装置F(如图所示,已略去夹持装置)。
①铜丝绕成螺旋状的作用是_________(填编号);
a.制取更多氧气 b.增大接触面 c.没有影响
②与装置B比较,改进后装置F的优点是_____________。
【答案】(1)①长颈漏斗 ②水槽
(2)B D
(3)2H2O2![]() 2H2O + O2↑ 在水中推上玻璃片 向上
2H2O + O2↑ 在水中推上玻璃片 向上
(4)①b ②可以随时控制反应
【解析】
试题分析:(2)实验室用锌和稀硫酸反应制取氢气,属固液在常温下的反应,选B装置;氢气的密度比空气小,故用向上排空气法收集,选D装置;
(3)过氧化氢分解生成的是水和氧气:2H2O2 ![]() 2H2O + O2↑;装置E是用排水法收集氧气,收集满后要在水槽中盖好玻璃片,正放在实验台上;
2H2O + O2↑;装置E是用排水法收集氧气,收集满后要在水槽中盖好玻璃片,正放在实验台上;
(4)铜丝绕成螺旋状可增大它与过氧化氢的接触面积;氧化铜能催化过氧化氢分解,当需要反应时,将铜丝推入过氧化氢溶液中;不需要反应时,将同时往上拉,氧化铜与过氧化氢分离,反应停止,即该反应可以随时控制反应的发生和停止。

 励耘书业暑假衔接宁波出版社系列答案
励耘书业暑假衔接宁波出版社系列答案【题目】育才中学的某研究小组在探究维生素C水溶液的酸碱性时,不慎误把维C泡腾片(保健品。主要成分如图所示)当做维生素C片放入了水中,结果发现有大量气泡产生,于是引起了该小组同学的探究兴趣。

【提出问题】该气体成分是什么?
【猜想与假设】小青说:该气体可能含有CO2 、 O2、 CO、 H2 、 N2 中的一种或几种。小丽说:不可能含有 N2,因为
小亮说:不可能含有H2 和CO,因为从药品安全角度考虑,H2易燃易爆,CO
最后研究小组的同学共同认为:该气体可能含有CO2、O2中的一种或两种。
【进行实验】
编号 | 实验操作 | 实验现象 |
① | 将气体通入澄清的石灰水 | 澄清石灰水变浑浊 |
② | 将带火星的木条伸入到该气体中 | 带火星的木条没有复燃 |
【得出结论】(1)由实验①可知,该气体中肯定含有 ,
(2)由实验② (填“能”或“不能”)确定该气体中不含氧气,理由是