题目内容
某化学兴趣小组为测定某黄铜样品(铜锌合金)中铜的含量,进行如图所示的实验。根据以下信息回答下列问题:
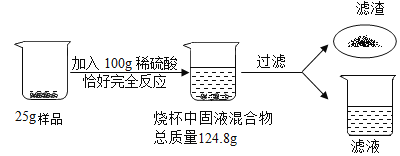
(1)写出实验中发生反应的化学方程式_____;
(2)根据已知条件列出求解生成硫酸锌质量(X)的比例式_____;
(3)该黄铜样品中铜的质量分数为_____;
(4)若要使所得滤液中溶质的质量分数为10%,需加入水的质量为_____;
(5)若用98%的浓硫酸配制所用的稀硫酸,则需要浓硫酸的质量为_____;
(6)若工业上用含Cu2S 80%的辉铜矿111t(炼制过程中辉铜矿的损失率为20%),能炼出上述黄铜的质量为_____。
练习册系列答案
 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案
相关题目
对下列事实的解释不正确的是( )
选项 | 事 实 | 解 释 |
A | 宝石绚丽多彩 | 宝石中含有某些金属原子 |
B | 蔗糖放入水中会“消失” | 蔗糖分子在水分子的作用下分散到水分子之间 |
C | 在溶液中反应的速率快 | 反应时大量分子或离子同时直接接触 |
D | 一氧化碳和二氧化碳的化学性质不同 | 分子的构成不同 |
A.A B.B C.C D.D


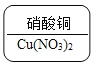 B.
B.
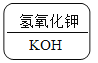 D.
D.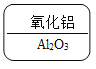
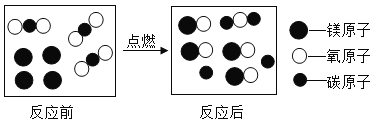
 和
和 的微粒个数比是4:3
的微粒个数比是4:3 是由原子构成的单质,只有
是由原子构成的单质,只有 属于氧化物
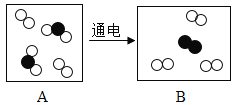
属于氧化物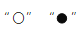 分别表示氢原子、氧原子,如图是电解水时发生反应的微观模拟图。请回答:
分别表示氢原子、氧原子,如图是电解水时发生反应的微观模拟图。请回答: