题目内容
【题目】两个烧杯中装有等质量的金属锌和铁,然后分别逐渐加入同种浓度的稀硫酸,产生氢气的质量与加入硫酸的质量关系如图所示。下列说法正确的是
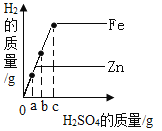
A.铁和锌产生氢气的速率一样快
B.加入cg硫酸时,两个烧杯中的酸都恰好完全反应
C.加入bg硫酸时,两个烧杯中产生氢气的质量相同
D.加入ag硫酸时,两个烧杯中都有金属剩余
【答案】D
【解析】
根据铁、锌金属活动性均比氢强,均能与稀硫酸反应,等质量的金属锌和铁,分别逐渐加入同浓度的稀硫酸,由产生氢气的质量与加入硫酸的质量关系图,最终铁产生的氢气质量多,进行分析判断.
A、锌的金属活动性比铁,锌产生氢气的速率比铁快,故选项说法错误。
B、加入cg硫酸时,铁与稀硫酸恰好完全反应,锌已经过量,锌与稀硫酸不是恰好完全反应,故选项说法错误。
C、加入bg硫酸时,铁产生的氢气多,锌产生的氢气质量少,故选项说法错误。
D、加入ag硫酸时,硫酸全部参加反应,两个烧杯中都有金属剩余,故选项说法正确。
故选:D。

练习册系列答案
相关题目
【题目】以下是日常生活中常用的各种清洗剂,试回答:
洗涤灵 | 洁厕灵 | 炉具清洁剂 | 活氧彩漂 | 污渍爆炸盐 |
|
|
|
|
|
功能:清除油污 | 有效成分:盐酸 | 有效成分:氢氧化钠 | 有效成分:过氧化氢 | 有效成分:过碳酸钠 |
(1)使用洗涤灵清洗餐具上的油污,这是因为洗涤灵具有_______作用
(2)以下物质中,可使用洁厕灵清除的是_______。(填字母序号)
①内壁沾有硫酸钡沉淀的试管 ②油污 ③水垢
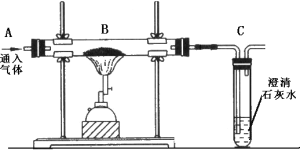
(3)污渍爆炸盐溶于水后生成Na2CO3和H2O2,再加入足量洁厕灵,产生能使澄清石灰水变浑浊的气体,此反应体现了下图中_______ (选填“①”“②”“③”“④”)性质关系。
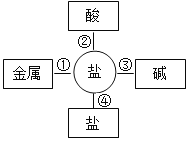
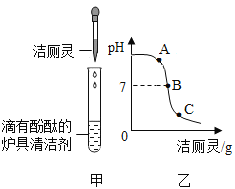
(4)将洁厕灵滴入炉具清洁剂中,如下图所示。若反应后溶液呈红色,此时溶液可用下图中______(选填A、B、C)点处表示。