题目内容
【题目】(6分)根据下列所示装置,结合所学知识回答问题。

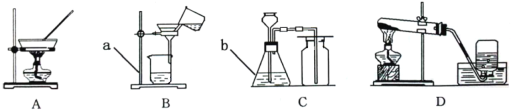
(1)用A装置制取氧气,反应的化学方程式是___________________________________。
(2)用B装置收集氧气,当看到有_____________________时开始收集;当看到集气瓶口有
时说明已收集满。
(3)C装置中充满水时,可作为氧气的收集装置,则氧气应从 (填“a”或“b”)端通入。
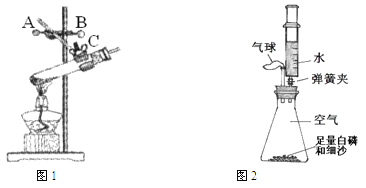
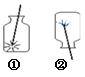
(4)按下图所示,将带火星的木条分别插入盛满氧气的集气瓶中,观察到木条复燃,且在①中燃烧比在②中旺。以上实验现象说明了氧气的性质:① ;
② 。
【答案】(1)2KMnO4△ K2MnO4 + MnO2 + O2↑;(2)连续气泡冒出 ; 大气泡冒出;(3)b ; (4)①支持燃烧; ②密度比空气大
【解析】
试题分析: (1)A装置是固体加热型装置,且试管口有一团棉花,所以是高锰酸钾制氧气,方程式为2KMnO4△K2MnO4+MnO2↑;(2)用排水法收集氧气时,必须要等到气泡均匀连续冒出时,再收集.当瓶口有气泡向外冒出时,说明氧气收集满了;(3)C装置中充满水时,可作为氧气的收集装置,氧气的密度比水小,要短进长出;(4)木条都能复燃说明氧气能支持燃烧;在A中能燃烧的更旺说明氧气聚集在集气瓶底部,从而证明氧气的密度比空气大。

 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案【题目】(7分)某同学做了如下图所示实验:
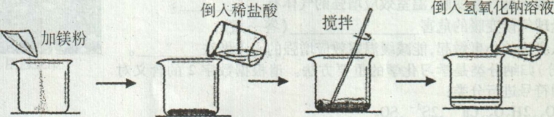
第一次 | 第二次 | |
加入镁粉的质量 | m | m |
加入质量分数为14.6%稀盐酸的质量 | 50g | lOOg |
加入氢氧化钠溶液的质量 | 100g | 100g |
加入氢氧化钠溶液后的实验现象 | 产生白色沉淀 | 无明显现象 |
第一次实验每步均恰好完全反应,请回答:
(1)写出第一次实验中发生反应的化学方程式___________________________;
(2)第二次反应后溶液中溶质的组成是___________________________;
(3)每次实验中加入镁的质量(m)为___________________________;
(4)求解第一次反应中生成气体的质量(X)的比例式为___________________________;
(5)若将第一次反应后溶液蒸发掉68.4g水后,则所得不饱和溶液中溶质的质量分数___________;
(6)若用36.5%的浓盐酸配制实验中所需稀盐酸,则需要加水的质量为_______________。