题目内容
【题目】(6分)
下列为配制100g质量分数为10.6%的碳酸钠溶液的实验,请分析有关问题:
(1)计算:碳酸钠的质量为 g,水为 g。
(2)称量:用托盘天平称量, 碳酸钠应放在 (填“左盘”或“右盘”)。
(3)溶解:用量筒来量取所需的水(水的密度为1g/cm3),,量筒的规格是 (从下列中选用:10mL、25 mL、50 mL、100 mL);溶解碳酸钠要用到玻璃棒,其作用是 。
(4)反思:若称取的碳酸钠中喊有水分,则所配制的溶液的质量分数会 (填“偏大”、“偏小”或“无影响”)。
【答案】(1)10.6 89.4 (2)左盘 (3)100Ml 加快溶解 (4)偏小
【解析】分析:(1)根据有关溶质质量分数的计算分析即可,溶质质量分数=![]() ×100%
×100%
(2)用托盘天平称量固体时,物体放在左盘,砝码放在右盘,
(3)量取液体体积时,所选量筒的规格应稍大于所需要的液体体积,
溶解固体时,为了加速其溶解,可以用玻璃棒搅拌,
(4)根据公式:溶质质量分数=![]() ×100%,若溶质质量减小则溶质质量分数减小.
×100%,若溶质质量减小则溶质质量分数减小.
解答:解:(1)∵溶质质量分数=![]() ×100%
×100%
∴溶质质量=溶液质量×溶质质量分数=100×10.6%=10.6g
溶剂质量=溶液质量-溶质质量=100-10.6=89.4g
故答案为:10.6; 89.4
(2)用托盘天平称量固体时应遵循“左物右码“的原则,
故答案为:左盘
(3)因为需要溶剂的体积为89.4ml,所选量筒的量程要稍大于所需水的体积,所以选100ml的量筒,
溶解碳酸钠时,用玻璃棒搅拌可以加速其溶解.
故答案为:100mL; 加快溶解
(4)因为溶质质量分数=![]() ×100%,所以若称取的碳酸钠中含有水分,即溶质质量减小,故溶质质量分数偏小,
×100%,所以若称取的碳酸钠中含有水分,即溶质质量减小,故溶质质量分数偏小,
故答案为:偏小

 阅读快车系列答案
阅读快车系列答案【题目】盐酸溶液中含有H2O分子、H+和Cl-,要探究是哪一种粒子能使紫色石蕊溶液变成红色,请观察在白色点滴板上进行的下列实验,将实验现象和结论填入下表。
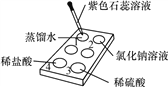
滴加紫色石蕊溶液后的现象 | 结论 | |
第1孔 | 孔中溶液仍为紫色 | 水分子_________________ |
第2孔 | ____________________ | _______________________ |
第3孔、第4孔 | ____________________ | _______________________ |