题目内容
(2008?沈阳)如图是固体物质甲的溶解度曲线,请据图回答下列问题.
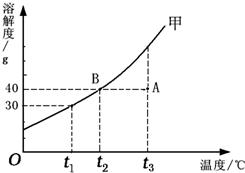
(1)t2℃时,甲的溶解度为
(2)t3℃时,若将40g甲物质放入到100g水中,充分溶解后,所得溶液在溶解度曲线图中可表示为

(1)t2℃时,甲的溶解度为
40
40
g.(2)t3℃时,若将40g甲物质放入到100g水中,充分溶解后,所得溶液在溶解度曲线图中可表示为
A
A
(填“A”或“B”)点,若将其降温到t1℃,能析出晶体10
10
g.分析:(1)利用溶解度曲线可以查找该物质在任意温度下的溶解度;
(2)溶解度曲线上的点对应的溶液均为饱和溶液,根据溶解度为该温度下,100g溶剂所能溶解溶质的最大质量,此时的饱和溶液中溶剂质量为100g、溶质质量即为此时的溶解度、溶液质量为(100+溶解度)g.
(2)溶解度曲线上的点对应的溶液均为饱和溶液,根据溶解度为该温度下,100g溶剂所能溶解溶质的最大质量,此时的饱和溶液中溶剂质量为100g、溶质质量即为此时的溶解度、溶液质量为(100+溶解度)g.
解答:解:(1)根据溶解度曲线可查得,t2℃时甲的溶解度为40g;
故答案为:40;
(2)根据溶解度曲线可知,t3℃时若将40g甲物质放入到100g水中,充分溶解后,所得溶液为不饱和溶液;溶解度曲线上的溶液为饱和溶液,不饱和溶液处于曲线下方,所以,图中A点表示该溶液;
故答案为:A;
将该溶液降温到t1℃,根据t1℃时甲物质的溶解度为30g,即此时100g水最多溶解30g甲达饱和,所以加入的40g固体甲只能溶解30g而有10g固体析出;
故答案为:10.
故答案为:40;
(2)根据溶解度曲线可知,t3℃时若将40g甲物质放入到100g水中,充分溶解后,所得溶液为不饱和溶液;溶解度曲线上的溶液为饱和溶液,不饱和溶液处于曲线下方,所以,图中A点表示该溶液;
故答案为:A;
将该溶液降温到t1℃,根据t1℃时甲物质的溶解度为30g,即此时100g水最多溶解30g甲达饱和,所以加入的40g固体甲只能溶解30g而有10g固体析出;
故答案为:10.
点评:溶解度曲线上的点表示该温度下,100g水溶解溶质达饱和状态时所形成的饱和溶液,溶质质量即此时的溶解度.

练习册系列答案
相关题目