题目内容
(2004?泰州)实验室里有一瓶常见的无色盐溶液因保管不当,标签残缺不全,只剩下“Na”字样.为确定此溶液的组成,请你做出一种假设,并按照你的假设填写下表,完成探究过程.| 假设溶液的成分 | 验证方法 | 能观察到的现象 | 结论 |
【答案】分析:根据无色盐溶液残缺标签上的“Na”字样可得知该溶液为钠盐的溶液;盐为金属与酸根组成的化合物,而常见的酸根有SO42-、CO32-、NO3-、Cl-;因此可假设钠盐为:Na2SO4、Na2CO3、NaNO3、NaCl;
根据SO42-、CO32-、Cl-三种酸根的检验方法,设计实验进行检验探究.
解答:解:硫酸根可与钡离子形成不溶于酸的硫酸钡沉淀,若假设为硫酸钠时,可加入氯化钡等可溶性钡盐及稀硝酸进行检验;碳酸根可与酸反应放出气体二氧化碳,若假设如碳酸钠时,可采取滴加稀盐酸并把产生气体通入澄清石灰水的方法进行检验;氯离子能与银离子形成不溶于酸的氯化银沉淀,若假设为氯化钠时,可采取滴加硝酸银溶液并滴加稀硝酸的方法进行检验;
故答案为:
点评:碳酸根的检验:取样滴加稀盐酸,产生气体通入澄清石灰水,石灰水变浑浊,则样品中含碳酸根;
硫酸根的检验:取样滴加酸化的硝酸钡溶液,出现白色沉淀,则样品中含有硫酸根;
氯离子的检验:取样滴加酸化的硝酸银溶液,出现白色沉淀,则样品中含有氯离子.
根据SO42-、CO32-、Cl-三种酸根的检验方法,设计实验进行检验探究.
解答:解:硫酸根可与钡离子形成不溶于酸的硫酸钡沉淀,若假设为硫酸钠时,可加入氯化钡等可溶性钡盐及稀硝酸进行检验;碳酸根可与酸反应放出气体二氧化碳,若假设如碳酸钠时,可采取滴加稀盐酸并把产生气体通入澄清石灰水的方法进行检验;氯离子能与银离子形成不溶于酸的氯化银沉淀,若假设为氯化钠时,可采取滴加硝酸银溶液并滴加稀硝酸的方法进行检验;
故答案为:
| 假设溶液的成分 | 验证方法 | 能观察到的现象 | 结论 |
| 硫酸钠溶液 | 取溶液,滴加氯化钡溶液,并滴入几滴稀盐酸 | 出现白色沉淀 | 盐溶液为硫酸钠溶液 |
| 碳酸钠溶液 | 取溶液,滴加稀盐酸,把气体通入澄清石灰水 | 产生气泡,澄清石灰水变浑浊 | 盐溶液为碳酸钠溶液 |
| 氯化钠溶液 | 取溶液,滴加硝酸银溶液,并滴入几滴稀硝酸 | 出现白色沉淀 | 盐溶液为氯化钠溶液 |
点评:碳酸根的检验:取样滴加稀盐酸,产生气体通入澄清石灰水,石灰水变浑浊,则样品中含碳酸根;
硫酸根的检验:取样滴加酸化的硝酸钡溶液,出现白色沉淀,则样品中含有硫酸根;
氯离子的检验:取样滴加酸化的硝酸银溶液,出现白色沉淀,则样品中含有氯离子.

练习册系列答案
相关题目
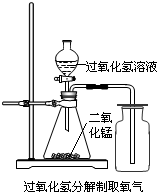 (2004?北碚区)实验室中,常采用分解过氧化氢溶液(二氧化锰作催化剂)或加热高锰酸钾的方法制取氧气.
(2004?北碚区)实验室中,常采用分解过氧化氢溶液(二氧化锰作催化剂)或加热高锰酸钾的方法制取氧气.