题目内容
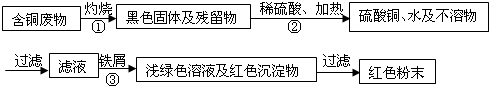
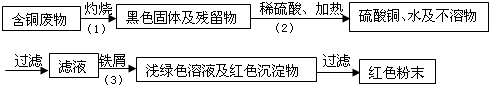
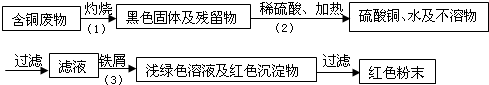
某市一家大型化工厂处理回收含铜废料的生产流程如图:
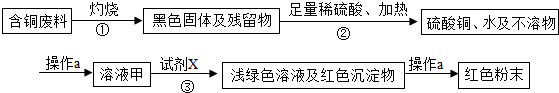
提示【过程①得到的残留物不溶于水和不溶于酸;过程②中黑色固体与足量稀硫酸、加热生成硫酸铜、水及不溶物】回答下列问题:
(1)写出流程①中与铜有关的化学方程式: .
(2)操作a的名称是 ,溶液甲呈 色.
(3)为达到回收铜的目的,流程③中加入的试剂X为 ,浅绿色溶液放在空气中一段时间后会变成黄色溶液请预测写出黄色溶液中含有的微粒有 (写出微粒符号).

提示【过程①得到的残留物不溶于水和不溶于酸;过程②中黑色固体与足量稀硫酸、加热生成硫酸铜、水及不溶物】回答下列问题:
(1)写出流程①中与铜有关的化学方程式:
(2)操作a的名称是
(3)为达到回收铜的目的,流程③中加入的试剂X为
分析:由流程图可知:铜和氧气在加热的条件下生成氧化铜,氧化铜和硫酸反应生成硫酸铜和水;不溶性固体与液体分开的方法叫过滤,因为铜离子是蓝色,因此硫酸铜溶液是蓝色的;流程③中加入过量的铁粉,铁与硫酸铜反应生成铜和硫酸亚铁,硫酸亚铁溶液是浅绿色,浅绿色溶液中主要含有的微粒有亚铁离子和硫酸根离子.
解答:解:(1)流程①中是铜和氧气在加热的条件下生成氧化铜,反应物是铜和氧气,生成物是氧化铜,所以化学方程式为:2Cu+O2
2CuO
(2)不溶性固体与液体分开的方法叫过滤,因为铜离子是蓝色,因此硫酸铜溶液是蓝色的;故答案为:过滤;蓝
(3)流程③中加入过量的铁粉,铁与硫酸铜反应生成铜和硫酸亚铁,硫酸亚铁溶液是浅绿色,浅绿色溶液中主要含有的微粒有亚铁离子和硫酸根离子;故答案为:Fe;Fe2+、SO42-;
故答案为:(1)2Cu+O2
2CuO;(2)过滤;蓝;(3)Fe;Fe2+、SO42-.
| ||
(2)不溶性固体与液体分开的方法叫过滤,因为铜离子是蓝色,因此硫酸铜溶液是蓝色的;故答案为:过滤;蓝
(3)流程③中加入过量的铁粉,铁与硫酸铜反应生成铜和硫酸亚铁,硫酸亚铁溶液是浅绿色,浅绿色溶液中主要含有的微粒有亚铁离子和硫酸根离子;故答案为:Fe;Fe2+、SO42-;
故答案为:(1)2Cu+O2
| ||
点评:有关实验方案的设计和对实验方案的评价是中考的热点之一,设计实验方案时,要注意用最少的药品和最简单的方法;关于对实验设计方案的评价,要在两个方面考虑,一是方案是否可行,能否达到实验目的;二是设计的方法进行比较,那种方法更简便

练习册系列答案
 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案
相关题目