题目内容
【题目】食品工业中合理使用食品添加剂可改善食品的色、香、味等品质.碳酸钠和碳酸氢钠就是食品中常用的添加剂,二者在不同温度时的溶解度如表所示
温度/℃ | 0 | 10 | 20 | 30 | 40 |
碳酸钠的溶解度/g | 7.1 | 12.5 | 21.5 | 39.7 | 49.0 |
碳酸氢钠的溶解度/g | 6.9 | 8.1 | 9.6 | 11.1 | 12.7 |
(1)10℃时,碳酸钠的溶解度为_____.
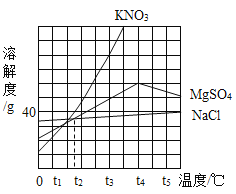
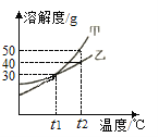
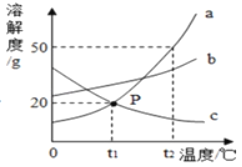
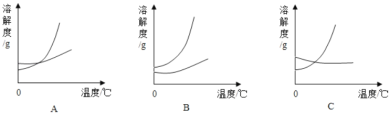
(2)两种物质的溶解度曲线关系合理的是_____.
(3)区分两种物质的方法:取两种固体粉末各xg加入20℃的10g水中充分溶解,通过观察现象可区分碳酸钠和碳酸氢钠,x的值可能是___(填字母),此时碳酸氢钠溶液中溶质的质量分数是___(精确到0.01%)
A 2 B 0.96 C 0.5
【答案】12.5g B A 8.76%
【解析】
(1)由溶解度表可以看出,10℃时,碳酸钠的溶解度为12.5g。
(2)碳酸氢钠的溶解度变化不如碳酸钠明显,且两种物质的溶解度不存在交点,故曲线关系合理的是B,故填:B.
(3)在20℃时,碳酸钠的溶解度为21.5g,碳酸氢钠的溶解度为9.6g,故要取两种固体粉末各xg加入20℃的10g水中充分溶解,通过观察现象可区分碳酸钠和碳酸氢钠,x的值应该介于2.15g和0.96g之间,故x可能是2,此时碳酸氢钠溶液中溶质的质量分数是
![]() ;故填:A;8.76%.
;故填:A;8.76%.

 名校课堂系列答案
名校课堂系列答案【题目】将“锡纸”剪成一段两头宽中间窄的纸条,然后两头分别连接电池的正负极,观察到“锡纸”立即燃烧。据此,小晟同学取某种“锡纸”进行了以下探究:
(1)“锡纸”燃烧的原因:“锡纸”两端接入电池两极后造成短路致使“锡纸”燃烧,从燃烧的条件开始“锡纸”不燃烧短路后却能燃烧的原因是_____。
(2)探究“锡纸”中金属的成分:“锡纸”中的金属是锡吗?
(查阅资料)①“锡纸”是锡箔或铝箔和纸粘合而成;②锌粉是一种深灰色固体;
③锡(Sn)与酸或盐溶液反应生成正二价的锡的化合物。
(提出猜想)猜想Ⅰ:“锡纸”中的金属是锡;猜想Ⅱ:“锡纸”中的金属是铝。
(进行实验)设计方案并进行实验
实验操作 | 实验现象 | 实验分析与结论 |
取打磨后的“锡纸”片放入试管中,滴加氯化锌溶液 | “锡纸”表面有深灰色固体析出 | 猜想_____(填“Ⅰ”或“Ⅱ”) 成立;反应的化学方程式为_____。 |
(交流讨论)①实验中打磨“锡纸”的目的是_____;
②下列物质的溶液可以替代氯化锌溶液完成上述实验的是_____(填序号)。
A 氯化铜 B 硝酸银 C 硫酸钠 D 硫酸亚铁
(拓展应用)如果电器着火下列采取的正确灭火方法是_____(填字母)。
A 立即用水扑灭 B 先切断电源,再用干粉灭火器灭火
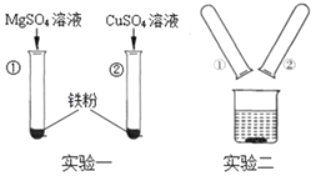
(3)小肖同学向MgSO4溶液、CuSO4溶液中分别加入铁粉(如图实验一),实验结束后,把①、②试管内的物质集中倒进一个烧杯中(如图实验二)。将实验二得到的物质进行过滤,向所得滤渣中加入稀盐酸,无气泡产生。则实验二得到的溶液中,溶质一定含有_____
(填化学式,下同),可能含有_____。
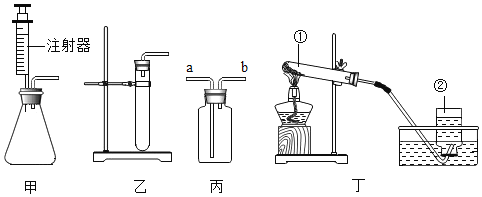
【题目】现有下列仪器或装置,请回答下列问题:
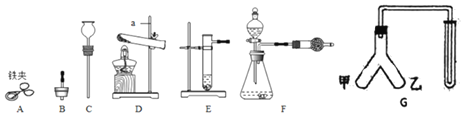
①仪器a的名称是______:用______![]() 填仪器名称
填仪器名称![]() 取废铁屑放入试管,可以用图A~E仪器组装成制取气体的发生装置:用废铁屑与稀盐酸反应制取H2,应选______
取废铁屑放入试管,可以用图A~E仪器组装成制取气体的发生装置:用废铁屑与稀盐酸反应制取H2,应选______![]() 填字母
填字母![]() ,写出反应的化学方程式:______。
,写出反应的化学方程式:______。
②选择气体收集方法时,必须考虑的气体性质有______![]() 填序号
填序号![]() 。
。
A 颜色 B 密度 C 溶解性 D 可燃性
③向“人”字型管G装置![]() 端分别装入一种固体和一种液体物质,按图示连接好装置,再倾斜装置,使乙中液体流入甲中。填写下表。
端分别装入一种固体和一种液体物质,按图示连接好装置,再倾斜装置,使乙中液体流入甲中。填写下表。
操作及现象 | 所装固体物质和液体物质 | 两端物质反应的化学方程式 |
将带火星木条放在试管口,木条复燃 | ______ | ______ |
将燃着木条放在试管口,木条熄灭 | ______ | ______ |
④若要检验F装置中产生的气体中是否含有水蒸气,干燥管中应该装入的物质是______。
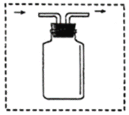
⑤若用如图装置且正放在桌上进行“排空气法”收集制取的H2,请把图中的“导气管”补画完整_____。