题目内容
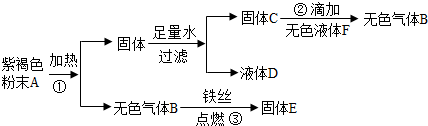
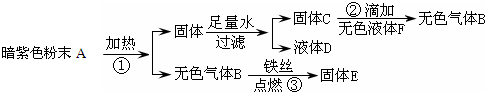
小刚同学在实验室中用一种紫黑色固体粉末A进行探究实验,他实验的过程和现象如图,请你帮其解决下列问题: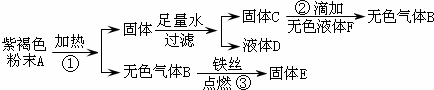
(1)写出下列物质的化学式并标出各元素化合价:B:
; F:
.
(2)反应①的化学方程式式为:

(1)写出下列物质的化学式并标出各元素化合价:B:
| +1+7-2 |
| KMnO4 |
| +1+7-2 |
| KMnO4 |
| +1-1 |
| H2O2 |
| +1-1 |
| H2O2 |
(2)反应①的化学方程式式为:
2KMnO4
K2MnO4+MnO2+O2↑
| ||
2KMnO4
K2MnO4+MnO2+O2↑
.该反应的基本反应类型为:
| ||
分解反应
分解反应
.反应③的化学方程式式为:3Fe+2O2
Fe3O4
| ||
3Fe+2O2
Fe3O4
,该反应的基本反应类型为:
| ||
化合反应
化合反应
.分析:本题的突破口是紫褐色粉末和反应③条件,根据无色气体B和铁丝燃烧生成固体E,可以推测B是氧气、固体E是四氧化三铁;根据反应①②和氧气的实验室制法可知,A是高锰酸钾、C是二氧化锰、F是水.
解答:解:(1)铁丝能够在无色气体B中燃烧,所以可以判断B为氧气,而固体E为四氧化三铁;固体C可以和A分解产生的固体反应生成氧气,所以可以判断F为过氧化氢,而固体C为二氧化锰,进而可以判断A为高锰酸钾,其中根据化合物正负化合价代数和为零,可以判断出高锰酸钾中各元素的化合价为:
;F为过氧化氢,其中氧元素的化合价为-1,即:
;
(2)根据(1)的解答可以知道反应为:2KMnO4
K2MnO4+MnO2+O2↑;该反应为分解反应;而反应为:3Fe+2O2
Fe3O4,该反应为化合反应.
故答案为:(1)
;
;
(2)2KMnO4
K2MnO4+MnO2+O2↑;分解反应;3Fe+2O2
Fe3O4,化合反应.
| +1+7-2 |
| KMnO4 |
| +1-1 |
| H2O2 |
(2)根据(1)的解答可以知道反应为:2KMnO4
| ||
| ||
故答案为:(1)
| +1+7-2 |
| KMnO4 |
| +1-1 |
| H2O2 |
(2)2KMnO4
| ||
| ||
点评:本题是一道综合性试题,既考查了学生对知识的整合能力同时又考查了学生进行实验探究的能力.

练习册系列答案
相关题目