题目内容
【题目】已知:通常情况下,二氧化碳不溶于饱和碳酸氢钠溶液.某实验小组据此设计了如图所示的实验装置研究用排水法能否收集二氧化碳的问题,其实验过程及结论如表: 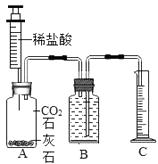
实验 | 实验过程 | 实验结果 |
1 | A中加入足量石灰石,并充满二氧化碳;B中盛满饱和碳酸氢钠溶液.将10mL稀盐酸注入瓶中. | 测得量实验2筒内液体体积比实验1少了约1%. |
2 | A中加入足量石灰石,并充满二氧化碳;B中盛满蒸馏水.将10mL稀盐酸(浓度与实验1相同)注入瓶中. |
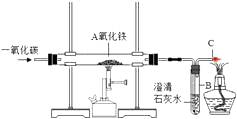
(1)实验开始时,A中充满二氧化碳的目的是 , A中发生反应的化学方程式为;
(2)该实验小组对比排水法收集气体的装置发现该实验装置有缺陷,为此对实验装置B进行了改进,改进的要点是;改进装置后,再次按照实验2的过程进行实验,结果发现:量筒内所得液体的体积比实验1少了约10%,其原因是;
(3)取实验2结束后B瓶中的溶液,向其中滴加紫色石蕊试液后振荡,溶液变色,其原因是(用化学方程式表示): .
【答案】
(1)避免空气对实验产生干扰;CaCO3+2HCl=CaCl2+H2O+CO2↑
(2)将装置B的左侧导管换成长导管并伸到集气瓶的底部;二氧化碳溶解速度慢,二氧化碳不会溶于水或与水反应
(3)红;H2O+CO2=H2CO3
【解析】解:(1)装置中的空气对体积的测定也会产生影响,所以A中充满二氧化碳的目的是:避免空气对实验产生干扰,碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,化学方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑;(2)二氧化碳溶于水,会与水反应,所以改进的方法是:将装置B的左侧导管换成长导管并伸到集气瓶的底部;通过分析可知,二氧化碳能用排水法收集的原因是:二氧化碳溶解速度慢,二氧化碳不会溶于水或与水反应;(3)水和二氧化碳反应生成碳酸,碳酸能使紫色石蕊变成红色,所以向其中滴加紫色石蕊试液后振荡,溶液变红色,其原因是:H2O+CO2=H2CO3 . 所以答案是:(1)避免空气对实验产生干扰,CaCO3+2HCl=CaCl2+H2O+CO2↑;(2)将装置B的左侧导管换成长导管并伸到集气瓶的底部;二氧化碳溶解速度慢,二氧化碳不会溶于水或与水反应;(3)红,H2O+CO2=H2CO3 .
【考点精析】认真审题,首先需要了解二氧化碳的化学性质(化学性质:一般情况下不能燃烧,也不支持燃烧,不能供给呼吸;与水反应生成碳酸;能使澄清的石灰水变浑浊;与灼热的碳反应),还要掌握书写化学方程式、文字表达式、电离方程式(注意:a、配平 b、条件 c、箭号)的相关知识才是答题的关键.

【题目】秸秆是农村的常见品,平均含硫量达千分之三点八(3.8‰),燃料后,其中的硫元素转化为SO2引起空气污染.假设我国空气质量标准对空气中二氧化硫的浓度级别规定如表所示(空气中二氧化硫的浓度用单位体积的空气中所含二氧化硫的质量表示).
浓度级别 | 标准(mg/m3) |
一级 | 浓度≤0.15 |
二级 | 0.15<浓度≤0.50 |
三级 | 0.50<浓度≤0.70 |
若某4m3空气恰好能与含碘(I2)5.08mg的碘水完全反应(该反应的化学方程式是:SO2+I2+2H2O=H2SO4+2HI),试通过计算说明此空气中二氧化硫的浓度级别.