题目内容
小王同学看到一则某化肥产品的广告,如图所示:
(1)小王通过计算发现该广告是虚假广告,请写出小王的计算过程和判断依据.

(2)小王认为该广告坑害农民,于是向有关部门反映技术监督局对该产品取样分析,测得该样品是氮元素的质量分数仅为28.0%,则该化肥中硝酸铵的质量分数是多少?
解:(1)纯硝酸铵中氮的质量分数为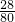 ×100%=35%<37.5%,故可判断该广告是虚假广告.
×100%=35%<37.5%,故可判断该广告是虚假广告.
(2)28%÷35%×100%=80%.
答:化肥中硝酸铵的质量分数是80%.
分析:(1)根据元素的质量分数公式计算出纯硝酸铵中氮的质量分数,再与广告上的含氮量做比较,即可知道该广告是虚假广告;
(2)根据质量分数公式即可计算出该化肥中硝酸铵的质量分数.
点评:本题主要考查学生运用质量分数公式计算的能力.
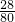 ×100%=35%<37.5%,故可判断该广告是虚假广告.
×100%=35%<37.5%,故可判断该广告是虚假广告.(2)28%÷35%×100%=80%.
答:化肥中硝酸铵的质量分数是80%.
分析:(1)根据元素的质量分数公式计算出纯硝酸铵中氮的质量分数,再与广告上的含氮量做比较,即可知道该广告是虚假广告;
(2)根据质量分数公式即可计算出该化肥中硝酸铵的质量分数.
点评:本题主要考查学生运用质量分数公式计算的能力.

练习册系列答案
相关题目
某同学对下列四个实验都设计了两种方案,两种方案均正确的是
| 实验 | 实验目的 | 方法和所加试剂 | |
| 方法一 | 方法二 | ||
| a | 区分CO和甲烷 | 用干冷烧杯检验燃烧产物 | 用涂有澄清石灰水烧杯检验燃烧产物 |
| b | 检验氯化钠中含有氢氧化钠 | 滴加酚酞溶液 | 加入盐酸 |
| c | 除去氯化钠溶液中的碳酸钠 | 加入盐酸 | 加入澄清石灰水 |
| d | 除去氯化钙溶液中的少量盐酸 | 加入碳酸钙 | 蒸发 |
- A.A、
- B.B、
- C.C、
- D.D、
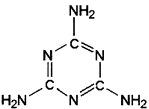 震惊全国的“三鹿奶粉”事件中的罪魁祸首是三聚氰胺(分子结构如图).三聚氰胺是一种重要的化工原料,由于其含氮量高,且目前国际上又通用“测氮法”标定牛奶中蛋白质含量,于是一些不法商人就将其混入奶粉中以“提高”奶粉的品质.
震惊全国的“三鹿奶粉”事件中的罪魁祸首是三聚氰胺(分子结构如图).三聚氰胺是一种重要的化工原料,由于其含氮量高,且目前国际上又通用“测氮法”标定牛奶中蛋白质含量,于是一些不法商人就将其混入奶粉中以“提高”奶粉的品质.