题目内容
某研究性学习小组的同学前往当地的石灰石矿区进行调查,他们取了若干块矿石样品,对样品中的碳酸钙的质量分数进行检测,采用了以下的办法:取用8 g这种石灰石样品,把40 g稀盐酸分四次加入,测量过程所得数据见下表(杂质不溶于水,不与盐酸反应)| 序号 | 第一次 | 第二次 | 第三次 | 第四次 |
| 加入稀盐酸质量g | 10 | 10 | 10 | 10 |
| 剩余固体质量g | 5.5 | m | 1.2 | 1.2 |
(2)上表中的m的数值应为多少?
(3)要得到280 Kg的CaO,需要质量分数为80%的石灰石多少千克?
分析:(1)比较第三次和的四次的数据可知:样品中杂质的质量为1.2g,结合样品的质量就可以计算出样品中碳酸钙的质量分数.
(2)比较第一次和第三次的数据可知第一次中盐酸完全反应,消耗碳酸钙8g-5.5g=2.5g,因此第二次中也是消耗2.5g碳酸钙,所以用第一次的剩余固体质量减去第二次消耗的碳酸钙的质量就是第二次剩余固体的质量.
(3)由生成氧化钙的质量和石灰石中碳酸钙的质量分数,根据碳酸钙分解的化学方程式就可以计算出需要石灰石的质量.
(2)比较第一次和第三次的数据可知第一次中盐酸完全反应,消耗碳酸钙8g-5.5g=2.5g,因此第二次中也是消耗2.5g碳酸钙,所以用第一次的剩余固体质量减去第二次消耗的碳酸钙的质量就是第二次剩余固体的质量.
(3)由生成氧化钙的质量和石灰石中碳酸钙的质量分数,根据碳酸钙分解的化学方程式就可以计算出需要石灰石的质量.
解答:解:(1)样品中碳酸钙的质量分数为
×100%=85%
(2)m=5.5g-(8g-5.5g)=3g
(3)设需要石灰石的质量为x.
CaCO3
CaO+CO2↑
100 56
x×80% 280Kg
=
,x=625Kg
答:(1)样品中碳酸钙的质量分数为85%,
(2)m的数值为3,
(3)需要石灰石的质量为625kg.
| 8g-1.2g |
| 8g |
(2)m=5.5g-(8g-5.5g)=3g
(3)设需要石灰石的质量为x.
CaCO3
| ||
100 56
x×80% 280Kg
| 100 |
| 56 |
| x×80% |
| 280Kg |
答:(1)样品中碳酸钙的质量分数为85%,
(2)m的数值为3,
(3)需要石灰石的质量为625kg.
点评:本题主要考查含杂质物质的化学方程式的计算,难度较大.

练习册系列答案
 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案
相关题目
(2009?天河区一模)某研究性学习小组的学生在学习完分子的特征后,做了如下两个实验,请按要求填空:
| 实验步骤 | 实验现象 | 实验结论或解释 |
| 实验一:在两个相同的茶杯内分别注入同体积的凉开水,一只杯子里加一小匙蜂蜜(主要成分是果糖),另一只杯子里加一小匙白醋(主要成分是醋酸),立即尝两只杯子里的水. | 放蜂蜜的杯子里的水基本不甜,放白醋的杯子里的水很酸. | ______分子的运动的速度比______分子的运动速度快,这说明相对分子质量越小的物质其分子的运动速度就______.(填“快”或“慢”)(提示:醋酸分子的相对分子质量比果糖分子的相对分子质量小.) |
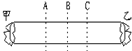
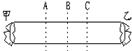
实验二:如图所示的玻璃管两端甲、乙两处分别放着蘸有浓氨水和浓盐酸的棉花. | 在______处出现较多白烟(填A或B或C). | 浓氨水挥发出来的氨分子(NH3)和浓盐酸挥发出来的氯化氢分子(HCl )接触时会产生大量的白烟. |
25.(2009?天河区一模)某研究性学习小组的学生在学习完分子的特征后,做了如下两个实验,请按要求填空:
| 实验步骤 | 实验现象 | 实验结论或解释 |
| 实验一:在两个相同的茶杯内分别注入同体积的凉开水,一只杯子里加一小匙蜂蜜(主要成分是果糖),另一只杯子里加一小匙白醋(主要成分是醋酸),立即尝两只杯子里的水. | 放蜂蜜的杯子里的水基本不甜,放白醋的杯子里的水很酸. | ______分子的运动的速度比______分子的运动速度快,这说明相对分子质量越小的物质其分子的运动速度就______.(填“快”或“慢”)(提示:醋酸分子的相对分子质量比果糖分子的相对分子质量小.) |
实验二:如图所示的玻璃管两端甲、乙两处分别放着蘸有浓氨水和浓盐酸的棉花. | 在______处出现较多白烟(填A或B或C). | 浓氨水挥发出来的氨分子(NH3)和浓盐酸挥发出来的氯化氢分子(HCl )接触时会产生大量的白烟. |