题目内容
含有杂质的镁2.4g放入一定量盐酸中,得到0.202g氢气,该镁中可能混有的杂质是( )A.锌
B.铁
C.铝
D.铜
【答案】分析:金属与酸发生置换反应的条件:(1)对金属的要求:必须是金属活动性顺序中排在氢以前的金属;(2)对酸的要求:这里所指的酸并不是所有的酸,主要是指稀盐酸和稀硫酸.
金属与酸反应产生H2的规律:
(1)H2的质量=金属的质量×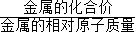
(2)等质量的几种金属与足量酸反应产生的H2质量与 的值成正比,该值越大,产生的H2质量越多,该值越小,产生的H2质量越小.
的值成正比,该值越大,产生的H2质量越多,该值越小,产生的H2质量越小.
解答:解:2.4g克纯镁放在足量的稀盐酸中 放出的氢气是0.2克,存在杂质导致生成的氢气的质量变大,即相同质量金属杂质比镁生成的氢气质量要多;
化学方程式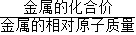
Zn+2HCl═ZnCl2+H2↑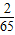
Mg+2HCl═MgCl2+H2↑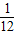
2Al+6HCl═2AlCl3+3H2↑
Fe+2HCl═FeCl2+H2↑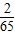
所以相同质量的锌、镁、铝、铁与足量的盐酸反应,生成氢气的质量大小为铝>镁>铁>锌;而铜不与盐酸反应;
故选C.
点评:本题是有关物质中的所含杂质的推断计算题,解答时,常采用极端假设法和平均值法,来进行分析、探究和计算.但是,一定要细心认真,切不可马虎大意.
金属与酸反应产生H2的规律:
(1)H2的质量=金属的质量×
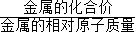
(2)等质量的几种金属与足量酸反应产生的H2质量与
 的值成正比,该值越大,产生的H2质量越多,该值越小,产生的H2质量越小.
的值成正比,该值越大,产生的H2质量越多,该值越小,产生的H2质量越小.解答:解:2.4g克纯镁放在足量的稀盐酸中 放出的氢气是0.2克,存在杂质导致生成的氢气的质量变大,即相同质量金属杂质比镁生成的氢气质量要多;
化学方程式
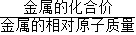
Zn+2HCl═ZnCl2+H2↑
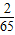
Mg+2HCl═MgCl2+H2↑
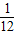
2Al+6HCl═2AlCl3+3H2↑

Fe+2HCl═FeCl2+H2↑
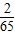
所以相同质量的锌、镁、铝、铁与足量的盐酸反应,生成氢气的质量大小为铝>镁>铁>锌;而铜不与盐酸反应;
故选C.
点评:本题是有关物质中的所含杂质的推断计算题,解答时,常采用极端假设法和平均值法,来进行分析、探究和计算.但是,一定要细心认真,切不可马虎大意.

练习册系列答案
相关题目