题目内容
【题目】(8分)
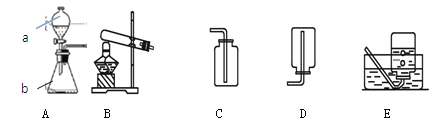
某化学兴趣小组使用下图所示装置,对某种锌铜合金的成分进行测量。先取足量稀硫酸于烧杯中,再向其中加入15.0g合金样品开始计时,并将电子天平的读数记录在下表中,完成下列计算:

(1)反应完全后产生氢气的质量是多少?
(2)锌铜合金中铜的质量是多少?
(3)反应完全后溶液中溶质的质量分数是多少?
空烧杯 | 加入硫酸后 | 加入合金后 5分钟 | 加入合金后 10分钟 | 加入合金后 30分钟 | |
读数(g) | 21.3 | 169.7 | 184.6 | 184.3 | 184.3 |
【答案】(1)0.4g (2)2g (3)20%
【解析】
试题分析:数据分析处理,加入硫酸后的质量为169.7g,再向其中加入15.0g合金样品,则开始反应的总质量为:169.7g+15.0g=184.7g,随着反应的进行,不断产生氢气,质量不断减少,直至质量不再发生变化,表示反应结束(1)根据质量守恒定律,产生氢气的质量=184.7g-184.3g=0.4g
(2)根据化学反应:Zn + H2SO4 === ZnSO4 + H2↑中氢气与锌的质量关系,即可求出锌的质量,反应后所得的溶液是ZnSO4溶液,通过氢气与ZnSO4的质量关系,即可求出ZnSO4的质量,进而可求反应完全后溶液中溶质的质量分数
解:设设合金中Zn的质量为x,生成的ZnSO4质量为y
Zn+H2SO4=ZnSO4+H2↑
65 161 2
x y 0.4g
65∶x =2∶0.4 g x=13 g
161∶y=2∶0.4 g y=32.2g
(2)锌铜合金中铜的质量为:15g-13 g=2g
(3)烧杯中溶液的质量为:184.3g-2g-21.3g=161.0g
∴ 反应完全后溶液中溶质的质量分数=32.2g/161g×100%=20%

 期末好成绩系列答案
期末好成绩系列答案 99加1领先期末特训卷系列答案
99加1领先期末特训卷系列答案 百强名校期末冲刺100分系列答案
百强名校期末冲刺100分系列答案 好成绩1加1期末冲刺100分系列答案
好成绩1加1期末冲刺100分系列答案 金状元绩优好卷系列答案
金状元绩优好卷系列答案【题目】 有一种神奇的蜡烛,点燃后任你怎么吹也吹不灭,而且看上去和普通的蜡烛一模一样,
到底是什么玄机能让蜡烛持续燃烧?请你一起参与探究。

【查阅资料】普通蜡烛由石蜡和蜡烛芯制成的,而吹不灭的蜡烛是在蜡烛芯上包裹一层打火石的粉末。打火石是由某种金属掺入少量稀土元素制成的合金,它的着火点只
有150℃。当蜡烛燃烧时,金属并不燃烧;但当蜡烛吹灭后,未冷却的金属接触到氧气就发生燃烧,从而使蜡烛复燃。
【探究与反思】这种蜡烛燃烧时,蜡烛芯里的金属为什么不燃烧? ,这种蜡烛也可以熄灭,你采用的方法是 。
【实验探究】吹不灭的蜡烛芯内的金属可能是镁、铝、铁或铜中的一种,为确定该金属的成分,请你继续探究并完成下列有关问题:(注:不考虑打火石中稀土元素对探究金属性质的影响)
实验 | 操作步骤 | 现象 | 结论 |
1 | 切开蜡烛,取出打火石,用砂纸打磨 | 打火石是银白色 | |
2 | 该金属一定不是铁 | ||
3 | 取少量打磨后的打火石于试管中,滴加硫酸铜溶液。 | 有红色物质析出 | 该金属一定是镁 |
【分析思考】
(1)请写出“实验3”中可能涉及到的化学方程式 。
(2)有同学认为通过“实验3”中现象不能证明烛芯内的金属一定是镁,因为 。
(3)针对以上实验,请你设计一个合理的实验方案来进一步验证这种金属,
操作步骤 | 现象 | 结论 |