题目内容
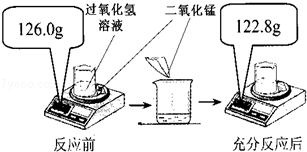
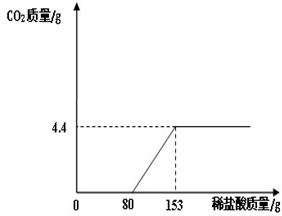
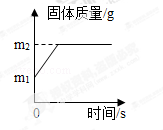
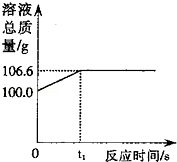
某造纸厂排放的废水中含有Na2CO3和NaOH,为了测定废水中Na2CO3的质量分数,取废水100g,逐滴加入稀盐酸至过量,测得生成气体质量与所加稀盐酸质量关系如图所示:
请回答下列问题:
(1)反应生成的气体质量为 g;与废水中NaOH反应掉的盐酸量为: ;
(2)该废水中Na2CO3的质量分数和所用稀盐酸溶质的质量分数。

请回答下列问题:
(1)反应生成的气体质量为 g;与废水中NaOH反应掉的盐酸量为: ;
(2)该废水中Na2CO3的质量分数和所用稀盐酸溶质的质量分数。
(1)4.4;80g;(2)废水中Na2CO3的质量分数是10.6%,所用稀盐酸溶质的质量分数为10%
试题分析:(1)根据图象可知生成二氧化碳的质量;同时也可以知道氢氧化钠先与稀盐酸反应(开始没有生成气体),从图象可知氢氧化钠消耗盐酸的质量。由图示可知生成二氧化碳的质量为4.4g;由图象可知氢氧化钠先与稀盐酸反应,方程式是:NaOH+HCl═NaCl+H2O;且两者恰好反应时消耗盐酸的质量是80g;
(2)根据二氧化碳的质量算出碳酸钠的质量,再用碳酸钠的质量除以废水的质量乘以百分之百,然后根据二氧化碳的质量计算出与碳酸钠反应的氯化氢的质量,用氯化氢的质量除以与碳酸钠反应的盐酸的质量乘以百分之百。设生成4.4g二氧化碳需要碳酸钠的质量为x,消耗氯化氢的质量为y
Na2CO3+2HCl═2NaCl+H2O+CO2↑
106 73 44
x y 4.4g
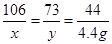
解得x=10.6g、y=7.3g
废水中Na2CO3的质量分数:
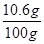 ×100%=10.6%;
×100%=10.6%;所用稀盐酸溶质的质量分数:
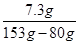 ×100%=10%;
×100%=10%;
练习册系列答案
相关题目
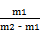
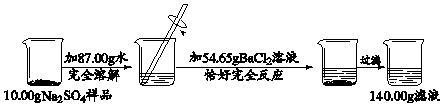
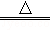 2CuSO4+ 2H2O
2CuSO4+ 2H2O  C2H4+4H2O.若用24g H2转化CO2,则理论上能生成C2H4的质量为多少克?
C2H4+4H2O.若用24g H2转化CO2,则理论上能生成C2H4的质量为多少克?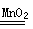 O2↑+2H2O.请计算:
O2↑+2H2O.请计算: