题目内容
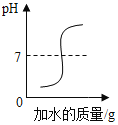
【题目】食盐在生产和生活中具有广泛的用途,是一种重要的资源,海水中储量很丰富,通过晾晒海水可以得到粗盐和卤水.如图所示为NaCl及卤水主要成分的溶解度曲线图.
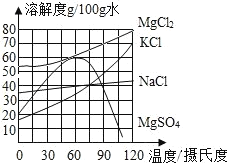
(1)海水晒盐的原理是_____;
(2)60℃时,100g水中加入80gKCl,充分搅拌后观察到的现象是_____.所形成的溶液是_____溶液(填“饱和”或“不饱和”).
(3)90℃时,MgCl2溶液的最大浓度(溶质质量分数)为_____(只列计算式,不需要计算结果).
(4)将90℃时,MgCl2、KCl和MgSO4三种物质的饱和溶液分别降温至30℃时,没有晶体析出的是_____(填物质名称).
【答案】利用阳光和风蒸发水分,使海水中的水分蒸发掉,使氯化钠结晶出来 有部分 KCl 未溶解 饱和溶液 ![]() MgSO4
MgSO4
【解析】
(1)食盐的溶解度受温度的影响小,从食盐溶液中获得食盐主要利用阳光和风蒸发水分,使海水中的水分蒸发掉,使氯化钠结晶出来。
(2)由KCl的溶解度曲线可知,在60℃时,KCl的溶解度是35.5g,100g水中加
入80gKCl,充分搅拌后观察到的现象是有部分KCl未溶解,所形成的溶液是饱和
溶液。
(3)由MgCl2的溶解度曲线可知,在90℃时,MgCl2溶液的溶解度是70g,在
90℃时,MgCl2饱和溶液的浓度最大,为:![]() 。
。
(4)将90℃时,MgCl2、KCl和MgSO4三种物质的饱和溶液分别降温至30℃时,由于MgSO430℃时溶解度大于90℃时的溶解度,没有晶体析出。
故答案为:(1)利用阳光和风蒸发水分,使海水中的水分蒸发掉,使氯化钠结晶出来.(2)有部分KCl未溶解,饱和溶液;(3)![]() ;(4)MgSO4。
;(4)MgSO4。

练习册系列答案
相关题目