题目内容
【题目】某研究性学习小组探究CuSO4溶液与NaOH溶液的反应产物。
(1)两溶液混合生成蓝色沉淀的化学方程式是_______________________。沉淀放置一段时间后,完全变为黑色沉淀,猜想是CuO。为验证猜想,将沉淀过滤、洗涤、烘干后,用CO还原得到红色物质,且生成的气体能使_____________________,写出CO与CuO反应的化学方程式:____________________________。
(2)CuSO4溶液与NaOH溶液反应有时也会生成Na2SO4和浅绿色沉淀[化学式为CuSO4·3Cu(OH)2],则反应的化学方程式为_________________。
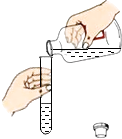
(3)为探究新制Cu(OH)2的分解温度,设计水浴加热装置(如图所示)。
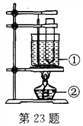
写出仪器的名称:①_________,②___________。该装置采用水浴加热,其目的是______________________。
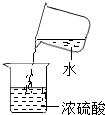
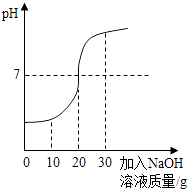
(4) 18℃时,将溶质质量分数均为10%的CuSO4溶液与NaOH溶液混合后,测得混合液温度为22℃,说明该反应_______(填“放热”或“吸热”)。当水浴温度分别为30℃、60℃、90℃时,黑色沉淀出现的时间为:2分钟、6秒、1秒,则说明温度越高,Cu(OH)2分解速率越_______(填,“快”或“慢”)。该实验说明,Cu(OH)2分解温度______________(填“无确定数值”或“有确定数值”)。
【答案】 CuSO4+2NaOH=Cu(OH)2↓+Na2SO4 澄清石灰水变浑浊 CO+CuO![]() Cu+CO2 4CuSO4+6NaOH=CuSO4·3Cu(OH)2↓+3Na2SO4 烧杯 酒精灯 使试管受热均匀 放热 快 无确定数值
Cu+CO2 4CuSO4+6NaOH=CuSO4·3Cu(OH)2↓+3Na2SO4 烧杯 酒精灯 使试管受热均匀 放热 快 无确定数值
【解析】本题是信息题,考查了碱的化学性质,实验探究物质变化的条件和影响物质变化的因素等。根据实验现象进行分析。
(1)CuSO4溶液与NaOH溶液发生复分解反应生成Cu(OH)2和Na2SO4,其化学方程式是:CuSO4+2NaOH=Cu(OH)2↓+Na2SO4, CO还原CuO生成铜和CO2,CO2使澄清的石灰水变浑浊.其化学方程式是:CO+CuO![]() Cu+CO2;
Cu+CO2;
(2)依题意得:4CuSO4+6NaOH═CuSO43Cu(OH)2↓+3Na2SO4
(3)图中①②的仪器名称分别为:烧杯,酒精灯,采用水浴加热的目的一般是使反应物受热均匀,反应才能平稳快速进行;
(4)两种物质反应后温度升高,说明反应过程放出热量,水浴温度越高,黑色沉淀出现的时间越短,可得一般规律是温度越高,反应速度越快,不同的温度下氢氧化铜能分解,故Cu(OH)2分解温度无确定数值。

 阅读快车系列答案
阅读快车系列答案【题目】将一定量的苯(C6H6)和氧气置于一个完全封闭的容器中引燃,反应生成二氧化碳、水和一种未知物 X.测得反应前后物质的质量见表:
物质 | 苯 | 氧气 | 二氧化碳 | 水 | X |
反应前质量/g | 3.9 | 9.6 | 0 | 0 | 0 |
反应后质量/g | 0 | 0 | 6.6 | 2.7 | m |
下列判断正确的是( )
A.表中 m 的值为 13.5
B.该反应属于分解反应
C.物质 X 可能含有氢元素
D.物质 X 中一定含有碳元素