题目内容
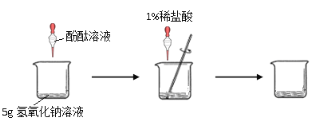
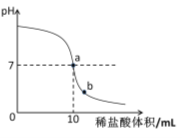
【题目】(7分)化学兴趣小组同学发现实验台上按如下顺序摆放着7瓶不同的无色溶液(如图所示),其中4、5号试剂瓶标签破损。
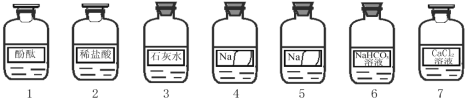
【提出问题】这两瓶试剂分别是什么?
【查阅资料】
①碱性的亚硫酸钠(Na2SO3)溶液、Na2CO3溶液都能与中性的CaCl2溶液发生复分解反应,产生白色沉淀。
②Na2SO3+2HCl=2NaCl+SO2↑+H2O。
③CO2与SO2均可以使澄清石灰水变浑浊,SO2是一种有刺激性气味的气体。
【作出猜想】4、5号溶液可能分别是NaOH、Na2CO3、Na2SO3或NaCl溶液中的一种。
【实施方案】取少量4、5号溶液分别于试管中,然后分别进行下列三组实验。
实验1:在两支试管中分别滴入上述七种溶液中的 号溶液,两试管中的溶液均变成红色,说明4、5号溶液均不可能是上述猜想中的 溶液。
实验2:在两支试管中分别滴入上述七种溶液中的3号溶液,两试管中均产生白色沉淀,4、5号溶液可能分别是Na2SO3溶液和Na2CO3溶液中的一种。写出其中一个反应的化学方程式 。
实验3:在两支试管中分别滴入上述七种溶液中的2号溶液,在盛4号溶液的试管中有 现象,说明4号是Na2CO3溶液;在盛5号溶液的试管中有 现象,说明5号是Na2SO3溶液。
【实验反思】同学们经过分析,认为4号溶液还可能是变质的NaOH溶液。请你利用上述图中的试剂设计鉴定实验方案,完成实验报告。
实验操作 | 实验现象 | 实验结论 |
4号溶液是部分变质的NaOH溶液。 |
【答案】[实施方案]
实验1: 1(1分) NaCl(或氯化钠)(1分)
实验2: Na2CO3 + Ca(OH)2 = CaCO3↓+ 2NaOH(或Na2SO3 + Ca(OH)2 = CaSO3↓+ 2NaOH)(1分)
实验3: 无色无味气体产生(1分) 刺激性气味的气体产生(1分)
[实验反思]
实验操作 | 实验现象 | |
①取少量4号溶液于试管中,加入足量CaCl2溶液 | ①有白色沉淀生成 | 每步操作和现象均答全者给1分,共2分 |
②向上层清液中滴加无色酚酞试液 | ②溶液由无色变成红色 |
【解析】
试题分析:【实施方案】实验1:NaOH、Na2CO3、Na2SO3三种溶液均呈碱性,都能使酚酞试液变为红色,说明4、5号溶液均不可能是上述猜想中的氯化钠溶液;实验2:根据碱与盐反应生成新碱和新盐,即可写出化学方程式;实验3:碳酸钠与稀盐酸反应,产生二氧化碳气体,说明4号是碳酸钠溶液;亚硫酸钠与稀盐酸反应,生成二氧化硫,二氧化硫具有刺激性气味,说明5号是Na2SO3溶液;[实验反思]氢氧化钠与二氧化碳反应生成碳酸钠而变质,碳酸钠与酸反应会产生气泡;碳酸钠与氯化钙反应,生成碳酸钙沉淀;碳酸钠溶液呈碱性,可以使酸碱指示剂变色等。

 学练快车道快乐假期寒假作业系列答案
学练快车道快乐假期寒假作业系列答案