题目内容
为了除去氯化钠样品中的碳酸钠杂质,兴趣小组最初设计了如下的方案并进行实验.
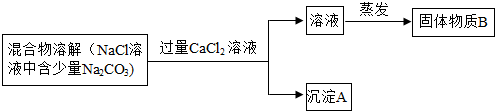
(1)写出沉淀A的化学式______.
(2)加入CaCl2溶液后,分离除去沉淀A的实验操作方法是______.
(3)同学在实验过程中,又发现了新的问题:此方案很容易引入新的杂质,请写出固体物质B的成分______(用化学式表示).
(4)同学继续探究后又提出新的方案:将混合物溶解,若滴加盐酸至不再产生气体为止,则既能除去Na2CO3杂质,又能有效地防止新杂质的引入.写出有关反应的化学方程式:______.
解:(1)碳酸钠和氯化钙反应生成碳酸钙和氯化钠,碳酸钙难溶于水,故答案为:CaCO3,
(2)加入氯化钙后生成了不溶于水的碳酸钙沉淀和氯化钠,要将沉淀分离出来,需要过滤,故答案为:过滤,
(3)加入的氯化钙是过量的,反应后的溶液中存在剩余的氯化钙和反应生成的氯化钠,故答案为:NaCl、CaCl2
(4)碳酸钠和盐酸反应生成水、氯化钠和二氧化碳,故答案为:Na2CO3+2HCl=2NaCl+H2O+CO2↑
分析:(1)根据碳酸钠和氯化钙的反应原理及生成物进行分析,
(2)根据过滤是将固体从溶液中分离的一种操作进行分析,
(3)根据加入的除杂试剂的量以及生成物进行分析,
(4)根据反应物、生成物书写化学方程式.
点评:在做物质的除杂题时,要搞清除需要除去的离子,在选择适当的试剂将其沉淀,当加入的试剂的状态和杂质状态相同时,要注意加入量的控制.
(2)加入氯化钙后生成了不溶于水的碳酸钙沉淀和氯化钠,要将沉淀分离出来,需要过滤,故答案为:过滤,
(3)加入的氯化钙是过量的,反应后的溶液中存在剩余的氯化钙和反应生成的氯化钠,故答案为:NaCl、CaCl2
(4)碳酸钠和盐酸反应生成水、氯化钠和二氧化碳,故答案为:Na2CO3+2HCl=2NaCl+H2O+CO2↑
分析:(1)根据碳酸钠和氯化钙的反应原理及生成物进行分析,
(2)根据过滤是将固体从溶液中分离的一种操作进行分析,
(3)根据加入的除杂试剂的量以及生成物进行分析,
(4)根据反应物、生成物书写化学方程式.
点评:在做物质的除杂题时,要搞清除需要除去的离子,在选择适当的试剂将其沉淀,当加入的试剂的状态和杂质状态相同时,要注意加入量的控制.

练习册系列答案
相关题目




