题目内容
将m克氢氧化钠固体完全溶于43.8克水中,将所得到的溶液加入到a克硫酸铜溶液中恰好完全反应,并得到溶质的质量分数为10%的溶液.反应时生成沉淀的质量与硫酸铜溶液质量的关系如图所示.求,(1)氢氧化钠固体的质量
(2)恰好反应时所得到的溶质的质量分数为10%的溶液质量.
(3)加入的硫酸铜溶液的质量.
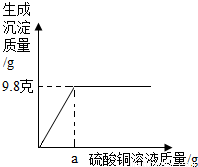
【答案】分析:(1)从图可以看出,m克氢氧化钠和a克硫酸铜溶液中的硫酸铜恰好反应时生成9.8g氢氧化铜沉淀,可以根据氢氧化铜的质量和化学方程式CuSO4+2NaOH=Na2SO4+Cu(OH)2↓可计算出氢氧化钠的质量;
(2)所得溶液中的溶质是硫酸钠,根据生成的沉淀的质量计算出生成的硫酸钠的质量,然后根据溶液中溶质的质量分数是10%,利用质量分数公式可求出所得溶液的质量;
(3)根据质量守恒定律可知,加入的硫酸铜溶液的质量等于反应后所得溶液的质量加上生成沉淀的质量减去氢氧化钠的质量再减去水的质量43.8g.
解答:解:从图可以看出,m克氢氧化钠和a克硫酸铜溶液中的硫酸铜恰好反应时生成9.8g氢氧化铜沉淀.氢氧化钠固体的质量为m,设生成硫酸钠的质量为x,则
CuSO4+2NaOH=Na2SO4+Cu(OH)2↓
80 142 98
m x 9.8g
(1)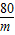 =
=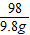 解得m=8g;
解得m=8g;
(2)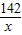 =
=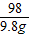 解得x=14.2g
解得x=14.2g
因此恰好反应时所得到的溶质的质量分数为10%的溶液质量为:14.2g÷10%=142g;
(3)根据质量守恒定律可知,加入的硫酸铜溶液的质量等于反应后所得溶液的质量加上生成沉淀的质量减去氢氧化钠的质量再减去水的质量43.8g,因此加入的硫酸铜溶液的质量为:142g+9.8g-8g-43.8g=100g.
答:(1)氢氧化钠固体的质量为8克;
(2)恰好反应时所得到的溶质的质量分数为10%的溶液质量为142g;
(3)加入的硫酸铜溶液的质量100g.
点评:本题是借助于数学模型,利用图表的方式来分析和解决化学计算中的有关问题,要求学生有较强的识图能力和数据分析能力.要求我们既能根据化学方程式进行溶质质量的计算,还要能根据质量守恒定律求出溶液的质量.
(2)所得溶液中的溶质是硫酸钠,根据生成的沉淀的质量计算出生成的硫酸钠的质量,然后根据溶液中溶质的质量分数是10%,利用质量分数公式可求出所得溶液的质量;
(3)根据质量守恒定律可知,加入的硫酸铜溶液的质量等于反应后所得溶液的质量加上生成沉淀的质量减去氢氧化钠的质量再减去水的质量43.8g.
解答:解:从图可以看出,m克氢氧化钠和a克硫酸铜溶液中的硫酸铜恰好反应时生成9.8g氢氧化铜沉淀.氢氧化钠固体的质量为m,设生成硫酸钠的质量为x,则
CuSO4+2NaOH=Na2SO4+Cu(OH)2↓
80 142 98
m x 9.8g
(1)
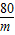 =
=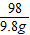 解得m=8g;
解得m=8g;(2)
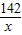 =
=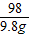 解得x=14.2g
解得x=14.2g因此恰好反应时所得到的溶质的质量分数为10%的溶液质量为:14.2g÷10%=142g;
(3)根据质量守恒定律可知,加入的硫酸铜溶液的质量等于反应后所得溶液的质量加上生成沉淀的质量减去氢氧化钠的质量再减去水的质量43.8g,因此加入的硫酸铜溶液的质量为:142g+9.8g-8g-43.8g=100g.
答:(1)氢氧化钠固体的质量为8克;
(2)恰好反应时所得到的溶质的质量分数为10%的溶液质量为142g;
(3)加入的硫酸铜溶液的质量100g.
点评:本题是借助于数学模型,利用图表的方式来分析和解决化学计算中的有关问题,要求学生有较强的识图能力和数据分析能力.要求我们既能根据化学方程式进行溶质质量的计算,还要能根据质量守恒定律求出溶液的质量.

练习册系列答案
相关题目
若将5克某物质完全溶于95克水中,所得溶液中的溶质的质量分数为( )
| A、等于5% | B、小于5% | C、大于5% | D、不能确定 |
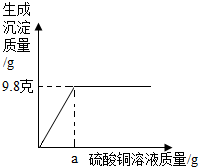 (2012?西藏二模)将m克氢氧化钠固体完全溶于43.8克水中,将所得到的溶液加入到a克硫酸铜溶液中恰好完全反应,并得到溶质的质量分数为10%的溶液.反应时生成沉淀的质量与硫酸铜溶液质量的关系如图所示.求,
(2012?西藏二模)将m克氢氧化钠固体完全溶于43.8克水中,将所得到的溶液加入到a克硫酸铜溶液中恰好完全反应,并得到溶质的质量分数为10%的溶液.反应时生成沉淀的质量与硫酸铜溶液质量的关系如图所示.求,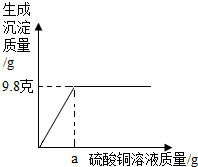 将m克氢氧化钠固体完全溶于43.8克水中,将所得到的溶液加入到a克硫酸铜溶液中恰好完全反应,并得到溶质的质量分数为10%的溶液.反应时生成沉淀的质量与硫酸铜溶液质量的关系如图所示.求,
将m克氢氧化钠固体完全溶于43.8克水中,将所得到的溶液加入到a克硫酸铜溶液中恰好完全反应,并得到溶质的质量分数为10%的溶液.反应时生成沉淀的质量与硫酸铜溶液质量的关系如图所示.求,