题目内容
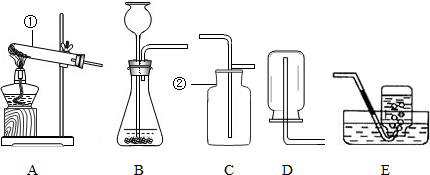
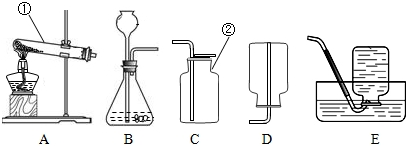
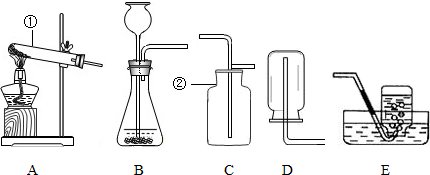
某同学在实验室组装了如图所示五种仪器装置,请根据要求回答下列问题.(可用序号填写的一律用序号)
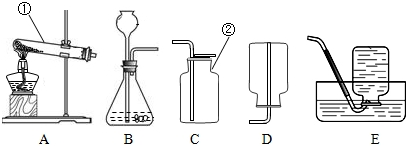
(1)写出装置中下列仪器的名称:①______,②______.
(2)若制取氧气,所需发生装置是______,收集装置是______,反应的化学方程式为______,此反应的类型属于______.
(3)制取氢气的发生装置是______,收集装置是______,反应的化学方程式是______,此反应的类型属于______.
(4)2003年12月,在重庆开县境内发生重大天然气井喷事故,造成人员重大伤亡.然而使许多村民中毒死亡的气体不是天然气,而是含在天然气中有毒的硫化氢(化学式为H2S)气体.硫化氢气体是无色、有臭鸡蛋气味、有毒的气体,
在标准状况下密度为1.518g/L;硫化氢气体充分燃烧可生成水和二氧化硫}通常状况下1体积水可溶解2.6体积的硫化氢气体,它的水溶液叫做氢硫酸.实验室常用固体硫化亚铁(FeS)和稀盐酸制取硫化氢气体,请写出反应的化学方程式______,并从上述五种仪器装置中选出制取硫化氢气体的发生装置为______,收集装置为______,请你根据介绍的硫化氢气体的物理、化学性质,为了防止污染,提出处理尾气的建议:______.
(5)在上面制取二氧化碳气体的实验中,若用去了含HCl 14.6g的盐酸,问理论上可制得CO2多少克?(请写出规范的解题步骤)

(1)写出装置中下列仪器的名称:①______,②______.
(2)若制取氧气,所需发生装置是______,收集装置是______,反应的化学方程式为______,此反应的类型属于______.
(3)制取氢气的发生装置是______,收集装置是______,反应的化学方程式是______,此反应的类型属于______.
(4)2003年12月,在重庆开县境内发生重大天然气井喷事故,造成人员重大伤亡.然而使许多村民中毒死亡的气体不是天然气,而是含在天然气中有毒的硫化氢(化学式为H2S)气体.硫化氢气体是无色、有臭鸡蛋气味、有毒的气体,
在标准状况下密度为1.518g/L;硫化氢气体充分燃烧可生成水和二氧化硫}通常状况下1体积水可溶解2.6体积的硫化氢气体,它的水溶液叫做氢硫酸.实验室常用固体硫化亚铁(FeS)和稀盐酸制取硫化氢气体,请写出反应的化学方程式______,并从上述五种仪器装置中选出制取硫化氢气体的发生装置为______,收集装置为______,请你根据介绍的硫化氢气体的物理、化学性质,为了防止污染,提出处理尾气的建议:______.
(5)在上面制取二氧化碳气体的实验中,若用去了含HCl 14.6g的盐酸,问理论上可制得CO2多少克?(请写出规范的解题步骤)
(1)根据实验室常用仪器的认识,可知仪器的名称为::①试管,②集气瓶;
(2)实验室制取氧气用“固体加热型”的装置;选取发生装置为A,依据氧气不易溶于水的性质选取收集装置为E;
制取氧气的反应方程式为:2KClO3
2KCl+3O2↑或 2KMnO4
K2MnO4+MnO2+O2↑;符合“一变多”
为分解反应;
(3)根据制取氢气用“固液常温型”的装置,氢气不溶于水,且密度比空气小,可以用排水法收集,因此制取氢气的发生装置是 B,收集装置是 D或E;
反应的化学方程式是;Zn+H2SO4=ZnSO4+H2↑;依据反应类型的判断该反应属于置换反应;
(4)根据题中信息:实验室常用固体硫化亚铁(FeS)和稀盐酸制取硫化氢气体,用“固液常温型”的装置,因此选用的发生装置为 B,收集装置为 C;
用固体硫化亚铁(FeS)和稀盐酸制取硫化氢气体的反应方程式为:2HCl+FeS=FeCl2+H2S↑;
依据硫化氢气体是无色、有臭鸡蛋气味、有毒的气体,将尾气通入NaOH溶液或气球收集或集气瓶收集;
(5)设理论上可制得C02的质量为x g
CaCO3 +2HC l=CaCl2 +H2O+CO2↑
73 44
14.6g x
=
解答 x=8.8
答:理论上可制得C02 8.8 g;
故答案为:(1)①试管;②集气瓶;
(2)A; E; 2KClO3
2KCl+3O2↑ 或 2KMnO4
K2MnO4+MnO2+O2↑;分解反应
(3)B;D或E; Zn+H2SO4=ZnSO4+H2↑;置换反应;
(4)2HCl+FeS=FeCl2+H2S↑; B; C;
通入NaOH溶液或气球收集或集气瓶收集.(若尾气用燃烧的方法处理则不得分);
(5)设理论上可制得C02的质量为x g
CaCO3 +2HCl=CaCl2 +H2O+CO2↑
73 44
14.6g x
=
解答 x=8.8
答:理论上可制得C02 8.8 g
(2)实验室制取氧气用“固体加热型”的装置;选取发生装置为A,依据氧气不易溶于水的性质选取收集装置为E;
制取氧气的反应方程式为:2KClO3
| ||
| △ |
| ||
为分解反应;
(3)根据制取氢气用“固液常温型”的装置,氢气不溶于水,且密度比空气小,可以用排水法收集,因此制取氢气的发生装置是 B,收集装置是 D或E;
反应的化学方程式是;Zn+H2SO4=ZnSO4+H2↑;依据反应类型的判断该反应属于置换反应;
(4)根据题中信息:实验室常用固体硫化亚铁(FeS)和稀盐酸制取硫化氢气体,用“固液常温型”的装置,因此选用的发生装置为 B,收集装置为 C;
用固体硫化亚铁(FeS)和稀盐酸制取硫化氢气体的反应方程式为:2HCl+FeS=FeCl2+H2S↑;
依据硫化氢气体是无色、有臭鸡蛋气味、有毒的气体,将尾气通入NaOH溶液或气球收集或集气瓶收集;
(5)设理论上可制得C02的质量为x g
CaCO3 +2HC l=CaCl2 +H2O+CO2↑
73 44
14.6g x
| 73 |
| 44 |
| 14.6 |
| x |
答:理论上可制得C02 8.8 g;
故答案为:(1)①试管;②集气瓶;
(2)A; E; 2KClO3
| ||
| △ |
| ||
(3)B;D或E; Zn+H2SO4=ZnSO4+H2↑;置换反应;
(4)2HCl+FeS=FeCl2+H2S↑; B; C;
通入NaOH溶液或气球收集或集气瓶收集.(若尾气用燃烧的方法处理则不得分);
(5)设理论上可制得C02的质量为x g
CaCO3 +2HCl=CaCl2 +H2O+CO2↑
73 44
14.6g x
| 73 |
| 44 |
| 14.6 |
| x |
答:理论上可制得C02 8.8 g

练习册系列答案
相关题目