题目内容
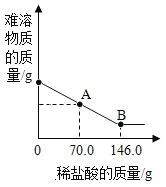
【题目】某地质勘探大队要测定某大理石样品中碳酸钙的质量分数,他们进行了如下实验:在烧杯中放入25.0 g大理石样品,向其中逐渐加入溶质质量分数为10%的稀盐酸,实验测得烧杯中难溶固体物质的质量与所滴入稀盐酸质量的关系曲线如图所示。(已知:大理石中的其他杂质不溶于水,且不与酸反应。)
请根据题意回答下列问题:
(1)在滴入稀盐酸的过程中,能观察到的明显现象有:①____________,②_____________。
(2)当滴入10%的稀盐酸至图中A点时,烧杯中溶液里的溶质是(写化学式)______________。
(3)当25.0 g大理石样品与稀盐酸充分反应后,理论上最终生成二氧化碳的质量为_________g。
(4)试计算:该大理石样品中碳酸钙的质量分数?__________________(计算结果精确至 0.1%)
【答案】固体逐渐减少 有气泡冒出 CaCl2 8.8 80.0%
【解析】
(1)碳酸钙与盐酸反应生成氯化钙、水和二氧化碳气体,所以可以看到固体逐渐减少,有气泡冒出;
(2)由图可知,图中A点时,盐酸不足,碳酸钙与盐酸反应生成氯化钙、水和二氧化碳气体,所以烧杯中溶液里的溶质氯化钙;
(3)B点时滴入稀盐酸中氯化氢的质量为:146.0g×10%=14.6g
设碳酸钙的质量为x,生成CO2的质量为y
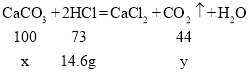
![]()
x=20.0g
![]()
y=8.8g
(4)大理石样品中碳酸钙的质量分数为![]() ×100%=80.0%。
×100%=80.0%。

练习册系列答案
 数学奥赛暑假天天练南京大学出版社系列答案
数学奥赛暑假天天练南京大学出版社系列答案 南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案
南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案
相关题目