题目内容
【题目】使用红磷燃烧的方法测定空气中氧气的含量:
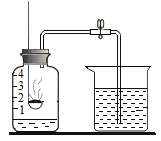
(1)写出红磷在空气中燃烧的化学方程式_______。
(2)在集气瓶中加入少量水,并将水面上方空间分成5等份,如图装置所示。待红磷熄灭并冷却后,打开弹簧夹,观察到烧杯中的水进入集气瓶,瓶内水面最终上升约至1刻度处。由此可知氧气约占空气总体积的____________。
(3)实验后发现测定空气中氧气含量偏低,造成这种结果的可能原因是:_____(填一种即可)。
(4)已知五氧化二磷溶于水且化学性质与二氧化碳相似,反应完毕后振荡集气瓶再滴入紫色石蕊溶液,溶液变_________色,说明该溶液显___________性。
【答案】4P+5O2 ![]() 2P2O5
2P2O5 ![]() 红磷不足(或装置漏气等合理答案即可) 红 酸
红磷不足(或装置漏气等合理答案即可) 红 酸
【解析】
(1)红磷在氧气中燃烧生成五氧化二磷,反应的化学方程式为:4P+5O2![]() 2P2O5;
2P2O5;
(2)红磷燃烧消耗氧气,打开弹簧夹时,烧杯中的水进入集气瓶,并且约占集气瓶容积的五分之一,所以可证明氧气约占空气总体积的![]() ;
;
(3)如果装置漏气或红磷的量不足或没有冷却到室温就打开止水夹读数等情况都可以使实验结果不准确,得出氧气体积含量低于五分之一的结论;
(4)紫色石蕊遇酸性溶液变红色,五氧化二磷溶于水且化学性质与二氧化碳相似,说明也能和水反应生成相应的酸,所以反应完毕后振荡集气瓶再滴入紫色石蕊溶液,溶液变红色,说明该溶液显酸性。

 阅读快车系列答案
阅读快车系列答案【题目】下列图像能正确反映对应变化关系的是( )
|
|
|
|
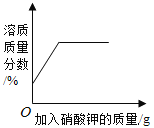
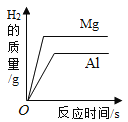
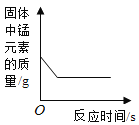
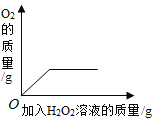
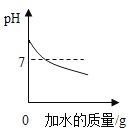
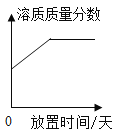
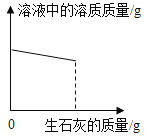
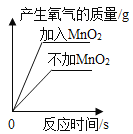
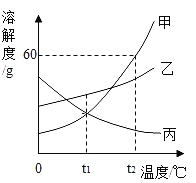
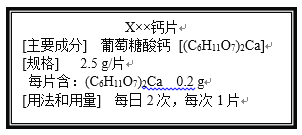
A 20℃时,向一定量的硝酸钾不饱和溶液中加入硝酸钾固体 | B将等质量的镁片和铝片投入到足量稀硫酸中 | C用酒精灯加热一定量的高锰酸钾固体 | D向盛有少量二氧化锰的烧杯中不断地加入过氧化氢溶液 |
A.AB.BC.CD.D
【题目】请回忆你学习过的“质量守恒定律”的实验探究,并按要求完成实验方案一和实验方案二。(下表中“实验结论”填“=”“>”或“<”)
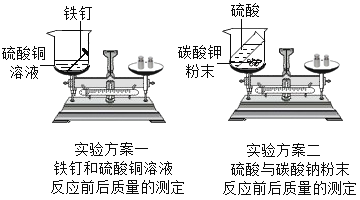
实验方案 | 方案一 | 方案二 |
反应现象 | 铁钉表面覆盖一层红色的物质,溶液由蓝色变成__________色 | 有气泡产生 |
化学方程式 | ________________ | H2SO4+K2CO3= K2SO4+CO2 |
反应前的总质量 | m1 | n1 |
反应后的总质量 | m2 | n2 |
实验结论 | m1_______m2 | n1________n2 |
将两个实验结果进行讨论对比时,有同学有一个方案观察到天平不平衡,是因为________,因此不能说质量不守恒。在反应物不变的前提下,要使天平平衡,你对该方案的改进措施是___________。