题目内容
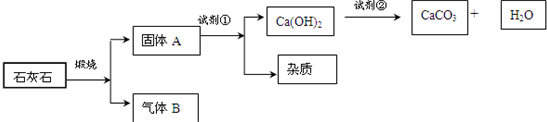
纯净的CaCO3可以用来测定盐酸的浓度.采用适当的试剂,从石灰石(主要成分是CaCO3)获得高纯度CaCO3的流程如下:

试回答:
①固体A是________;气体B是________;试剂①是________;试剂②是________.
②石灰石煅烧的化学方程式是________.
③使原料中各原子的利用率达到100%,是“绿色化学”的核心理念之一.上述流程中有的物质可以再利用,它是________.
生石灰 二氧化碳 水 二氧化碳 CaCO3 CaO+CO2↑ 二氧化碳或水
CaO+CO2↑ 二氧化碳或水
分析:①根据石灰石高温锻烧发生的分解反应,生成生石灰和二氧化碳,可判断A、B的成分;根据碳酸钙、生石灰与熟石灰之间的转化确定①、②的名称.
②石灰石的主要成分碳酸钙在高温下分解生成氧化钙和二氧化碳,写出反应的化学方程式即可.
③根据“绿色化学”的核心理念:使原料中各原子的利用率达到100%,判断流程图中还可以再利用的物质.
解答:①石灰石的主要成分碳酸钙在高温下分解生成氧化钙和二氧化碳,可知锻烧石灰石所得到的固体A是生石灰;气体B二氧化碳;生石灰与水反应生成氢氧化钙,故试剂①是水;氢氧化钙与水反应生成碳酸钙沉淀和水,故试剂②是二氧化碳.
②石灰石煅烧的化学方程式为:CaCO3 CaO+CO2↑.
CaO+CO2↑.
③石灰石的主要成分碳酸钙在高温下分解生成氧化钙和二氧化碳,二氧化碳与氢氧化钙反应生成碳酸钙和水,因此二氧化碳可以再利用;固体A需要与水反应生成氢氧化钙,而氢氧化钙与二氧化碳又生成了水,因此水也可以再利用.
故答案为:①生石灰;二氧化碳;水;二氧化碳;②CaCO3 CaO+CO2↑;③二氧化碳或水.
CaO+CO2↑;③二氧化碳或水.
点评:本题难度不是很大,掌握碳酸钙、生石灰与熟石灰之间的转化、理解“绿色化学”的核心理念是正确解答本题的关键.
 CaO+CO2↑ 二氧化碳或水
CaO+CO2↑ 二氧化碳或水分析:①根据石灰石高温锻烧发生的分解反应,生成生石灰和二氧化碳,可判断A、B的成分;根据碳酸钙、生石灰与熟石灰之间的转化确定①、②的名称.
②石灰石的主要成分碳酸钙在高温下分解生成氧化钙和二氧化碳,写出反应的化学方程式即可.
③根据“绿色化学”的核心理念:使原料中各原子的利用率达到100%,判断流程图中还可以再利用的物质.
解答:①石灰石的主要成分碳酸钙在高温下分解生成氧化钙和二氧化碳,可知锻烧石灰石所得到的固体A是生石灰;气体B二氧化碳;生石灰与水反应生成氢氧化钙,故试剂①是水;氢氧化钙与水反应生成碳酸钙沉淀和水,故试剂②是二氧化碳.
②石灰石煅烧的化学方程式为:CaCO3
 CaO+CO2↑.
CaO+CO2↑.③石灰石的主要成分碳酸钙在高温下分解生成氧化钙和二氧化碳,二氧化碳与氢氧化钙反应生成碳酸钙和水,因此二氧化碳可以再利用;固体A需要与水反应生成氢氧化钙,而氢氧化钙与二氧化碳又生成了水,因此水也可以再利用.
故答案为:①生石灰;二氧化碳;水;二氧化碳;②CaCO3
 CaO+CO2↑;③二氧化碳或水.
CaO+CO2↑;③二氧化碳或水.点评:本题难度不是很大,掌握碳酸钙、生石灰与熟石灰之间的转化、理解“绿色化学”的核心理念是正确解答本题的关键.

练习册系列答案
相关题目