题目内容
如图是 a、b、c 三种固体物质的溶解度曲线,下列分析不正确的是

A.t2℃时,a、b、c 三种物质的溶解度由大到小的顺序是 a>b>c
B.t1℃时,将 10ga 物质(不含结晶水)放入 50g 水中充分溶解可 得到 60ga 的饱和溶液
C.将 t2℃时,a、b、c 三种物质的饱和溶液降温至 t1℃,所得溶液 的溶质质量分数关系是 b>a=c
D.除去 a 中混有的少量 c 物质,可采取降温结晶的方法
CO2 通入 NaOH 溶液中无明显现象,为探究 CO2 与 NaOH 溶液是否发生了反应,某兴 趣小组进行了如下探究:
(查阅文献)(1)20℃时,几种物质在水中的溶解度见下表:
物质 | Na2CO3 | NaHCO3 | Ca(OH)2 | Ba(OH)2 |
溶解度/g | 21.5 | 9.6 | 0.165 | 3.89 |
(2)本实验条件下,Na2CO3 溶液和 NaHCO3 溶液的 pH 分别约为 11.0 和 8.5。
(3)Na2CO3可以和二氧化碳、水反应生成碳酸氢钠。
(实验探究)
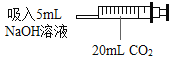
(1)实验一:小明用注射器抽取 20mLCO2,再抽取 5mLNaOH 溶液, 立即将针头插进橡皮塞中,振荡,发现注射器活塞左移,最后停在 10mL 刻度处,证明二氧化碳与氢氧化钠溶液发生了反应。小丽认为小明的结论不合理,又增加了一个实 验:_____(写出操作、现象),得出小明的结论正确。
(2)实验二:小明又取实验一所得溶液少许于试管中,向其中滴加BaCl2溶液,观察到______(填 现象),证明 CO2 与 NaOH 溶液发生了反应。实验中不宜将 BaCl2 溶液换成 CaCl2 溶液的原因是____________________。
(3)实验三:小明继续向实验二的溶液中滴加 BaCl2溶液至过量,静置,取上层清液,滴入 2 滴 酚酞试液,发现溶液呈___ 色,证明溶液中有 NaOH 剩余。实验中,小明没有直接取实验一的溶液 滴入酚酞试液,理由是__________________________________。
(反思感悟)对于现象不明显的化学反应,可以通过______________________来证明反应的发生。
(4)实验四:兴趣小组同学用如图 1 装置将 CO2 持续通入一定浓度一定量的 NaOH 溶液中,用数 字化实验技术测定反应过程中溶液的 pH 变化,结果如图 2 所示。

图 1 中,用纯碱与稀硫酸反应来制取二氧化碳,而不用大理石与盐酸反应来制取,理由是______________________________。最终溶液 pH 小于 8.5 的可能原因是__________________。CD 段发生反应的化学方程式为______________________________________。



 推广共享单车 B.
推广共享单车 B. 燃烧煤取暖
燃烧煤取暖 开私家车出行 D.
开私家车出行 D. 火力发电
火力发电 倾倒液体
倾倒液体 加热液体
加热液体 pH试纸使用
pH试纸使用 量取液体
量取液体