题目内容
【题目】(4分)某电镀厂排放的污水中含有CuSO4、ZnSO4、FeSO4,为减少水污染及节约成本,回收重要物质硫酸锌及有关金属,设计如下所示流程。
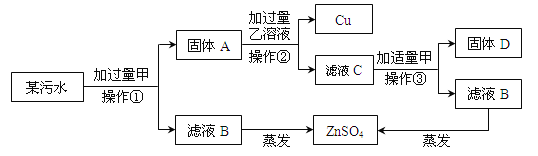
该回收流程中:固体A的成分是 ;含铁元素的物质(污水除外)有 (填字母序号),试写出滤液C与适量的甲发生的化学反应方程式 。
【答案】Cu、Fe、Zn(或铜、铁、锌) ACD FeSO4+Zn ZnSO4+Fe
【解析】
试题分析:根据为减少水污染及节约成本,回收重要物质硫酸锌及有关金属的目的,加入过量的甲物质为金属锌,故固体A中含有置换出的金属铜、铁,还有过量的金属锌;固体A中加入乙溶液为硫酸溶液,滤液C为硫酸亚铁溶液,固体D为金属铁,故 含铁元素的物质(污水除外)有ACD;写出滤液C与适量的甲发生的化学反应方程式FeSO4+Zn ZnSO4+Fe。

练习册系列答案
相关题目
【题目】下列叙述Ⅰ和叙述Ⅱ均正确,并且有因果关系的是( )
选项 | 叙述Ⅰ | 叙述Ⅱ |
A | Na2CO3溶液呈碱性 | Na2CO3属于碱 |
B | 铁可以和稀H2SO4反应放出H2 | Fe属于金属 |
C | 金属Al是热的良导体 | 金属Al可以用来制作生活炊具 |
D | 洗涤剂增大了油污在水中的溶解性 | 洗涤剂能除去衣服上的油污 |