题目内容
【题目】根据下列装置,结合所学化学知识回答问题。
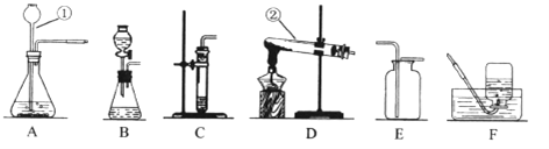
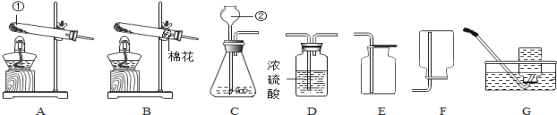
(1)写出上图所示装置中标有序号的仪器名称:①___________②____________。
(2)实验室中用氯酸钾制取氧气,发生反应的化学方程式____反应基本类型是____,制取气体时,组装好仪器后,应先___,再添加药品;如果需要随时控制产生气体的量,发生装置最好选用_____(填字母)。
(3)若要收集一瓶纯净的氧气,应选择收集装置________(填字母)。若选用如图装置收集氧气体时,气体应从__________端进。
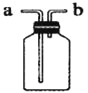
(4) 如用E装置收集氧气,检验氧气是否收集满的方法是________________
(5)已知甲烷是一种无色、无味的气体,密度比空气小,极难溶于水,实验室常用加热醋酸钠和氢氧化钠两种固体混合物的方法制取甲烷。实验室欲制取甲烷,可选上图装置中的______做发生装置,____做收集装置。
【答案】长颈漏斗 试管 2KClO3![]() 2KCl+3O2↑ 分解反应 检查装置的气密性 B F a 将带火星的木条伸到集气瓶口处,木条复燃,表明已经集满氧气 D F
2KCl+3O2↑ 分解反应 检查装置的气密性 B F a 将带火星的木条伸到集气瓶口处,木条复燃,表明已经集满氧气 D F
【解析】
(1)仪器①的名称是长颈漏斗,故填长颈漏斗;
仪器②的名称是试管,故填试管。
(2)氯酸钾在二氧化锰作催化剂和加热条件下反应生成氯化钾和氧气,故反应的化学方程式写为:2KClO3![]() 2KCl+3O2↑;
2KCl+3O2↑;
由化学方程式可知,该反应是一种物质反应生成两种物质,属于分解反应,故填分解反应;制取气体时,为防止气体逸散,组装好仪器后应检查装置的气密性,故填检查装置的气密性;装置B可通过调节分液漏斗的活塞控制滴加液体的速度,从而控制反应的速率,故选B。
(3)要收集一瓶纯净的氧气,应选择排水法,故填F;
因为氧气的密度大于空气的密度,所以氧气应该从长管进入瓶中,故填a。
(4)E装置为向上排空气法收集氧气,验满的方法是将带火星的木条伸到集气瓶口处,木条复燃,表明已经集满氧气,故填将带火星的木条伸到集气瓶口处,木条复燃,表明已经集满氧气。
(5)加热醋酸钠和氢氧化钠两种固体混合物的方法制取甲烷是加热固体生成气体,应选择固体受热发生装置,故填D;
甲烷的密度比空气小,且极难溶于水,所以收集甲烷既能用向下排空气法,也可以用排水法,故填F。

 小学数学口算题卡脱口而出系列答案
小学数学口算题卡脱口而出系列答案 优秀生应用题卡口算天天练系列答案
优秀生应用题卡口算天天练系列答案 浙江之星课时优化作业系列答案
浙江之星课时优化作业系列答案【题目】铁的化学性质比较活泼,能与氧气、酸、CuSO4溶液等多种物质发生化学反应。化学兴趣小组在课外资料中发现,铁和Fe2O3在高温条件下竟然也能发生化学反应。
(提出问题)
铁和Fe2O3反应的产物是什么?
(查阅资料)
①FeO、Fe2O3、Fe3O4中,Fe2O3是红棕色,其余是黑色;FeO在空气中会很快被氧化成Fe2O3;Fe3O4有磁性。②二氧化碳可用作该反应的保护气。③铁的氧化物都能与酸溶液反应。
(猜想与假设)
根据质量守恒定律,请你猜想铁和Fe2O3反应的产物:
①有FeO;②只有Fe3O4;③__________。
(进行实验)
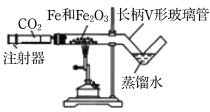
(1)按下图装好药品(铁粉过量),连好仪器(装入药品前已检查装置的气密性)。
(2)轻推注射器活塞通入二氧化碳,估计玻璃管里空气________,停止通入二氧化碳。
(3)点燃酒精喷灯加热药品,等到固体粉末全部变黑,再熄灭酒精喷灯。
(4)当长柄V形玻璃管冷却至室温时,检验黑色粉末成分。检验过程如下(请填写表格中的空白):
检验操作及现象 | 检验结果 | |
a | 黑色粉末暴露在空气中不变化 | 黑色粉末中一定没有___________ |
b | 用磁铁靠近,黑色粉末能完全被吸引 | 黑色粉末中一定含有铁和_______ |
c | 取少量的黑色粉末装入试管,滴加足量的___________溶液,出现红色固体,充分反应后仍残留少许黑色粉末 | 确认猜想_______正确 |
(探究结论)
铁和Fe2O3能发生化合反应,有关的化学方程式是________________。
(反思评价)
本实验中的保护气,既能用二氧化碳气体,也能用________________。