题目内容
某化合物1.5g完全燃烧,只生成4.4g二氧化碳和2.7g 水,则该化合物中
- A.只含碳、氢元素
- B.一定含碳、氢,可能含氧元素
- C.含碳、氢、氧元素
- D.氢元素质量分数20%
AD
分析:从题干分析计算后再去结合结果进行选项的分析与判断.计算的依据是质量守恒定律.
解答:某化合物1.5g完全燃烧,只生成4.4g二氧化碳和2.7g 水,生成的二氧化碳中含碳的质量为4.4g×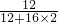 ×100%=1.2g.水中含氢元素的质量为2.7g×
×100%=1.2g.水中含氢元素的质量为2.7g× ×100%=0.3g.所以碳元素和氢元素的质量和为1.2g+0.3g=1.5g,等于该化合物的质量,说明该化合物不含氧元素,而只含碳元素和氢元素.
×100%=0.3g.所以碳元素和氢元素的质量和为1.2g+0.3g=1.5g,等于该化合物的质量,说明该化合物不含氧元素,而只含碳元素和氢元素.
A、根据分析计算,该化合物只含碳元素和氢元素.正确;
B、一定不含氧元素,错误;
C、不含氧元素.错误;
D、氢元素的质量分数等于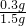 ×100%=20%.正确.
×100%=20%.正确.
故选A、D.
点评:给出数据的物质推断元素组成,不存在可能的问题,只有一定,所以B就是错误的.另外解答类似问题注意矛盾选项的问题,答案在矛盾中,A、B、C就是相互矛盾的,只会有一个正确.
分析:从题干分析计算后再去结合结果进行选项的分析与判断.计算的依据是质量守恒定律.
解答:某化合物1.5g完全燃烧,只生成4.4g二氧化碳和2.7g 水,生成的二氧化碳中含碳的质量为4.4g×
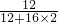 ×100%=1.2g.水中含氢元素的质量为2.7g×
×100%=1.2g.水中含氢元素的质量为2.7g× ×100%=0.3g.所以碳元素和氢元素的质量和为1.2g+0.3g=1.5g,等于该化合物的质量,说明该化合物不含氧元素,而只含碳元素和氢元素.
×100%=0.3g.所以碳元素和氢元素的质量和为1.2g+0.3g=1.5g,等于该化合物的质量,说明该化合物不含氧元素,而只含碳元素和氢元素.A、根据分析计算,该化合物只含碳元素和氢元素.正确;
B、一定不含氧元素,错误;
C、不含氧元素.错误;
D、氢元素的质量分数等于
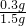 ×100%=20%.正确.
×100%=20%.正确.故选A、D.
点评:给出数据的物质推断元素组成,不存在可能的问题,只有一定,所以B就是错误的.另外解答类似问题注意矛盾选项的问题,答案在矛盾中,A、B、C就是相互矛盾的,只会有一个正确.

练习册系列答案
 波波熊暑假作业江西人民出版社系列答案
波波熊暑假作业江西人民出版社系列答案 学而优暑期衔接南京大学出版社系列答案
学而优暑期衔接南京大学出版社系列答案 Happy holiday欢乐假期暑假作业广东人民出版社系列答案
Happy holiday欢乐假期暑假作业广东人民出版社系列答案
相关题目